题目内容
右图是反应CO(g)+2H2(g)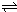 CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
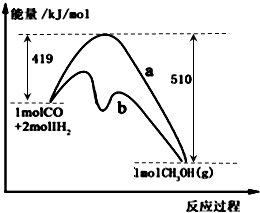
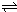 CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )| A.其它条件不变,按曲线b线进行的反应,CH3OH的产率更高 |
| B.其它条件不变,分别按曲线a、b线进行的反应的热效应相同 |
| C.(1molCO+2molH2)中的键能之和比1molCH3OH中的键能之和大 |
D.热化学方程式为CO(g)+2H2(g) CH3OH(g)△H=-91kJ?mol-1 CH3OH(g)△H=-91kJ?mol-1 |

A、曲线b表示使用催化剂后的能量变化,催化剂只改变所以速率,不改变化学平衡,所以反应物的转化率和生成物的产率不变,故A错误;
B、曲线a、b线进行的反应,b线使用催化剂降低了反应的活化能,改变了反应速率,但平衡开始和终了的物质能量未变,所以反应的热效应相同,故B正确;
C、图象中表示该反应是放热反应,所以拆化学键吸收的能量小于形成化学键所放出的能量,因此(1molCO+2molH2)中的键能之和比1molCH3OH中的键能之和小,故C错误;
D、图象中表示的是1molCO气体和2mol氢气反应生成1mol气态甲醇的反应热效应,反应放出热量=510KJ-419KJ=91KJ,根据热化学方程式的书写原则热化学方程式为:CO(g)+2H2(g) CH3OH(g)△H=-91kJ?mol-1,故D正确;
CH3OH(g)△H=-91kJ?mol-1,故D正确;
故选BD.
B、曲线a、b线进行的反应,b线使用催化剂降低了反应的活化能,改变了反应速率,但平衡开始和终了的物质能量未变,所以反应的热效应相同,故B正确;
C、图象中表示该反应是放热反应,所以拆化学键吸收的能量小于形成化学键所放出的能量,因此(1molCO+2molH2)中的键能之和比1molCH3OH中的键能之和小,故C错误;
D、图象中表示的是1molCO气体和2mol氢气反应生成1mol气态甲醇的反应热效应,反应放出热量=510KJ-419KJ=91KJ,根据热化学方程式的书写原则热化学方程式为:CO(g)+2H2(g)
 CH3OH(g)△H=-91kJ?mol-1,故D正确;
CH3OH(g)△H=-91kJ?mol-1,故D正确;故选BD.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
 +OH-====NH3·H2O
+OH-====NH3·H2O +5H+====Al(OH)3↓+Al3++H2O
+5H+====Al(OH)3↓+Al3++H2O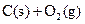 ══
══
 ══
══
 ══
══ △H= kJ/mol;
△H= kJ/mol;