题目内容
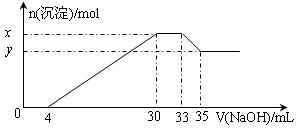
在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是
- A.原溶液中n(Mg2+)∶n(Al3+)=5∶2
- B.原溶液的pH=2
- C.x与y的差值为0.01 mol
- D.原溶液中c(Cl-)="0.75" mol·L-1
C
根据阳离子离子结合OH-的能力可知,氢氧化钠首先中和的是氢离子,则消耗氢氧化钠是4ml,然后与金属阳离子反应生成白色沉淀,最后与NH4+反应,消耗氢氧化钠是3ml。根据图像可知,溶解氢氧化铝消耗氢氧化钠是2ml,则生成氢氧化铝消耗氢氧化钠是6ml,所以生成氢氧化镁消耗的氢氧化钠是20ml,因此Mg2+、Al3+、NH4+、H+的物质的量分别是0.05mol、0.01mol、0.015mol、0.02mol,所以氯离子的物质的量是0.05mol×2+0.01mol×3+0.015mol+0.02mol=0.165mol,浓度是0.825mol/L,氢离子浓度是0.1mol/L,所以pH=1,因此正确的答案选C。
根据阳离子离子结合OH-的能力可知,氢氧化钠首先中和的是氢离子,则消耗氢氧化钠是4ml,然后与金属阳离子反应生成白色沉淀,最后与NH4+反应,消耗氢氧化钠是3ml。根据图像可知,溶解氢氧化铝消耗氢氧化钠是2ml,则生成氢氧化铝消耗氢氧化钠是6ml,所以生成氢氧化镁消耗的氢氧化钠是20ml,因此Mg2+、Al3+、NH4+、H+的物质的量分别是0.05mol、0.01mol、0.015mol、0.02mol,所以氯离子的物质的量是0.05mol×2+0.01mol×3+0.015mol+0.02mol=0.165mol,浓度是0.825mol/L,氢离子浓度是0.1mol/L,所以pH=1,因此正确的答案选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目