题目内容
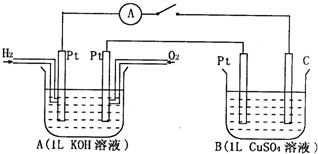
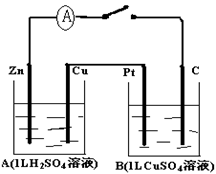
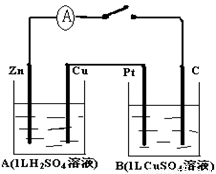
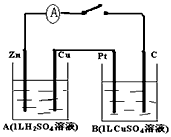
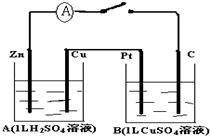 如图装置闭合电键时,电流计A的指针将发生偏转.试回答:
如图装置闭合电键时,电流计A的指针将发生偏转.试回答:(1)A池是
原电池
原电池
(填“原电池”或“电解池”)Cu的电极名称是正极
正极
(2)B池中的总反应化学方程式是
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
| ||
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
;若此过程中有0.02mol电子通过,则B中两极的质量差最多是
| ||
0.64
0.64
g(四个电极质量相同),B溶液的pH将
变小
变小
(填“变大”或“变小”).(3)如果要用B池给铁片上镀上一层Cu,则B池应作何改进
将B池中的Pt换成Cu,碳棒换成铁片
将B池中的Pt换成Cu,碳棒换成铁片
.分析:A为原电池,Zn为负极,发生氧化反应,Cu为正极,发生还原反应,B为电解池,Pt极为阳极,C极为阴极,电解时阳极生成氧气,阴极析出铜,以此解答该题.
解答:解:(1)A为原电池,Zn为负极,发生氧化反应,Cu为正极,发生还原反应,故答案为:原电池;正极;
(2)B为电解池,Pt极为阳极,C极为阴极,电解时阳极生成氧气,阴极析出铜,总反应化学方程式是2CuSO4+2H2O
2Cu+O2↑+2H2SO4,
阳极为C,电极质量无变化,阴极析出铜,质量增大,由Cu2++2e-=Cu,若此过程中有0.02mol电子通过,则生成0.01molCu,质量为0.64g,生成硫酸,则pH变小,
故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4;0.64;变小;
(3)如果要用B池给铁片上镀上一层Cu,形成电镀,铜作阳极,铁作阴极,则将B池中的Pt换成Cu,碳棒换成铁片,
故答案为:将B池中的Pt换成Cu,碳棒换成铁片.
(2)B为电解池,Pt极为阳极,C极为阴极,电解时阳极生成氧气,阴极析出铜,总反应化学方程式是2CuSO4+2H2O
| ||
阳极为C,电极质量无变化,阴极析出铜,质量增大,由Cu2++2e-=Cu,若此过程中有0.02mol电子通过,则生成0.01molCu,质量为0.64g,生成硫酸,则pH变小,
故答案为:2CuSO4+2H2O
| ||
(3)如果要用B池给铁片上镀上一层Cu,形成电镀,铜作阳极,铁作阴极,则将B池中的Pt换成Cu,碳棒换成铁片,
故答案为:将B池中的Pt换成Cu,碳棒换成铁片.
点评:本题综合考查原电池和电解池知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,有利于培养学生的良好的科学素养,难度不大,注意把握原电池和电解池的工作原理.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目