题目内容
| 时间(s) n(mol) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
②计算在80℃时该反应的平衡常数K=
③反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”、“变深”或“不变”)
④要增大该反应的K值,可采取的措施有(填序号)
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
⑤在同条件下,如果将0.40mol的N2O4气体充入2L已经抽空的固定容积的绝热密闭容器中,最终达到平衡后n(NO2)
②反应的平衡常数为生成物的浓度系数次幂之积除以反应物的浓度系数次幂之积所得的比值,由表中数据可知80s时,反应达平衡状态,计算出平衡时反应混合物各组分的物质的量,进而计算平衡时各组分的浓度,代入平衡常数表达式计算;
③该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小;
④平衡常数只受温度影响,要增大该反应的K值,应改变温度使平衡向正反应方向移动;
⑤反应开始四氧化二氮的物质的量相同,容器的体积相同,该反应正反应是吸热反应,在固定容积2L的绝热密闭容器,温度降低,平衡向逆反应移动,四氧化二氮的转化率降低.
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| 40s-20s |
②由表中数据可知80s时,反应达平衡状态,由(1)中计算可知d=e=0.1mol,故c(N2O4)=
| 0.1mol |
| 2L |
| 0.6mol |
| 2L |
| 0.32 |
| 0.05 |
③该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小,气体的颜色变浅,故答案为:变浅;
④平衡常数只受温度影响,要增大该反应的K值,应改变温度使平衡向正反应方向移动,该反应正反应是吸热反应,故应升高温度平衡向正反应移动,平衡常数k增大,故答案为:D;
⑤反应开始四氧化二氮的物质的量相同,容器的体积相同,该反应正反应是吸热反应,在固定容积2L的绝热密闭容器,温度降低,平衡向逆反应移动,四氧化二氮的转化率降低,故达到平衡时n(NO2)小于0.60mol,故答案为:<.

 全优点练单元计划系列答案
全优点练单元计划系列答案(6分)在80℃时,将0.40 mol N2O4气体充入2 L已经抽空的固定容积的密闭容器中发生反应N2O4(g)2NO2(g) △H= +57 kJ·mol-1,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4)/mol | 0.40 | a | 0.20 | c | d | e |
| n(NO2)/mol | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算a = ,此温度时该反应的平衡常数K= ;
(2)改变条件使反应重新达到平衡,能使c(NO2)/c(N2O4)值变小的措施有(填序号) 。
A.增大N2O4的起始浓度 B.升高温度
C.使用高效催化剂 D.向混合气体中通入稀有气体
(12分)在80℃时,将0.40 mol的N2O4气体充入1 L固定容积的密闭容器中发生反应:N2O4 2 NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4)(mol) | 0.40 | a | 0.20 | c | d | e |
| n(NO2)(mol) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)在20s — 40s之间,用N2O4表示的平均反应速率为 。
(2)在80℃时该反应的平衡常数K= 。
(3)要增大该反应的平衡常数,可采取的措施有(填序号) 。
①增大N2O4的起始浓度 ②向混合气体中通入NO2
③使用高效催化剂 ④升高温度
(4)反应进行至100s后若降低温度,混合气体的颜色 (填“变浅”、“变深”或“不变”)。
(5)反应进行至100s后若向容器中再充入0.40 mol的N2O4气体,则达到新平衡后N2O4的转化率将 (填“增大”、“减小”或“不变”)。
(6分)在80℃时,将0.40 mol N2O4气体充入2 L已经抽空的固定容积的密闭容器中发生反应N2O4(g) 2NO2(g)△H=" +57" kJ·mol-1,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g)△H=" +57" kJ·mol-1,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4)/mol | 0.40 | a | 0.20 | c | d | e |
| n(NO2)/mol | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)改变条件使反应重新达到平衡,能使c(NO2)/c(N2O4)值变小的措施有(填序号) 。
A.增大N2O4的起始浓度 B.升高温度
C.使用高效催化剂 D.向混合气体中通入稀有气体
(20分)在80 ℃时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4(g) 2NO2(g)ΔH >0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g)ΔH >0,隔一段时间对该容器内的物质进行分析,得到如下数据:
|
时间/s
n/mol |
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)计算20~40 s内用N2O4表示的平均反应速率为____________mol· L-1·s-1。
(2)计算在80 ℃时该反应的平衡常数K=___________。
(3)反应进行至100 s后将反应混合物的温度降低,混合气体的颜色___________(填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有___________(填序号)。
A.增大N2O4的起始浓度 B.向混合气体中通入NO
C.使用高效催化剂 D.升高温度
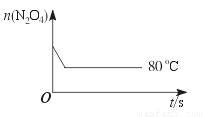
(5)如图是80 ℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60 ℃时N2O4物质的量的变化曲线。
(12分)在80℃时,将0.40 mol的N2O4气体充入1 L固定容积的密闭容器中发生反应:N2O4  2 NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
2 NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
|
时间(s) |
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4)(mol) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2)(mol) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)在20s — 40s之间,用N2O4表示的平均反应速率为 。
(2)在80℃时该反应的平衡常数K= 。
(3)要增大该反应的平衡常数,可采取的措施有(填序号) 。
①增大N2O4的起始浓度 ②向混合气体中通入NO2
③使用高效催化剂 ④升高温度
(4)反应进行至100s后若降低温度,混合气体的颜色 (填“变浅”、“变深”或“不变”)。
(5)反应进行至100s后若向容器中再充入0.40 mol的N2O4气体,则达到新平衡后N2O4的转化率将 (填“增大”、“减小”或“不变”)。