题目内容
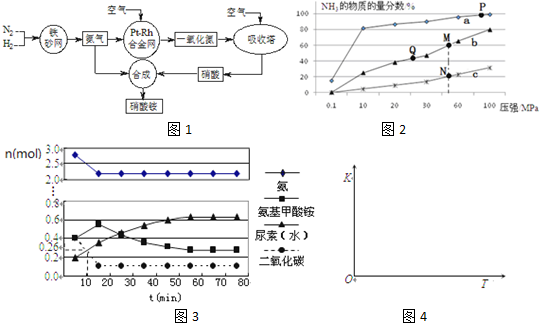
11.(1)工业制备硝酸流程如图1:
①上述尾气中的NO一定条件下可与氨气反应转化为氮气,则该反应的化学方程式为6NO+4NH3$\frac{\underline{\;一定条件\;}}{\;}$5N2+6H2O.
②某同学在实验室蒸馏含有Mg(NO3)2的稀硝酸制取浓硝酸,除导管、酒精灯、牛角管、锥形瓶、温度计、蒸馏烧瓶外,还需的玻璃仪器有冷凝管.
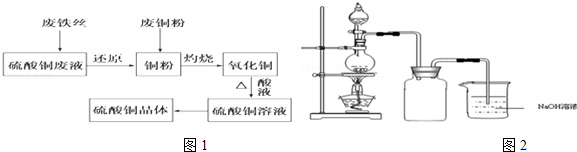
(2)某兴趣小组采用如图2装置制取并探究SO2气体的性质.
①下列实验方案适用于如图2所示装置制取所需SO2的是B(填序号)
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4
②将SO2通入到以下有颜色的溶液中,溶液的颜色均褪去,其中属于漂白的是C.
A.紫色高锰酸钾溶液 B.氯水 C.品经溶液 D.红色酚酞溶液
③证明c中生成气体是SO2,d中加入品红溶液后,打开活塞b,反应开始,待d中溶液红色褪去后,再加热(填实验的操作)试管d中的溶液,颜色又恢复,证明气体是SO2.
④指导老师指出应增加一尾气吸收装置,并帮助同学们设计了如装置如图3,其中合理的是A(填序号)
分析 (1)①NO一定条件下可与氨气反应转化为氮气和水,结合原子守恒配平书写得到化学方程式;
②依据蒸馏实验过程和实验装置分析需要的玻璃仪器;
(2)①实验室用Na2SO3 固体与浓硫酸反应制备二氧化硫气体;
②检验气密性,在连接好装置之后,可微热装置,观察是否有气泡冒出,并有一段水柱上升;
③根据二氧化硫气体的检验方法分析判断;
④依据尾气成分主要是二氧化硫选择吸收的试剂,装置中需要防止倒吸.
解答 解:(1)①NO一定条件下可与氨气反应转化为氮气,结合原子守恒配平书写得到化学方程式为:6NO+4NH3$\frac{\underline{\;一定条件\;}}{\;}$5N2+6H2O,
故答案为:6NO+4NH3$\frac{\underline{\;一定条件\;}}{\;}$5N2+6H2O;
②某同学在实验室蒸馏含有Mg(NO3)2的稀硝酸制取浓硝酸,除导管、酒精灯、牛角管、锥形瓶、蒸馏烧瓶、温度计外,还需的玻璃仪器有:冷凝管;
故答案为:冷凝管;
(2)①实验室用Na2SO3 固体与浓硫酸反应制备二氧化硫气体,而如图所示装置没有加热,则不能用浓硫酸和铜反应制备,
故答案为:B;
②A.SO2与紫色高锰酸钾溶液发生氧化还原反应,溶液的颜色均褪去;
B.SO2与氯水发生氧化还原反应,溶液的颜色均褪去;
C.SO2使品红溶液褪色,是因为二氧化硫有漂白性;
D.SO2溶于水,具有酸性,所以红色酚酞溶液褪色,
故选C;
③若要证明c中生成的气体是SO2,依据二氧化硫能使品红试液褪色,加热恢复红色;d中加入品红溶液后,打开活塞b,反应开始,待d中溶液红色褪去,再加热试管d中的溶液,颜色又恢复,证明气体是SO2,
故答案为:红色褪去; 加热;
④增加一尾气吸收装置防止污染性气体排放到空气中,装置需要很好地吸收气体,又能防止倒吸,BC易发生倒吸,D硫酸不能吸收二氧化硫,故选:A.
点评 本题考查了氮氧化物、硫及其化合物性质的应用,气体实验制备方法,装置注意问题,主要考查二氧化硫的氧化性,还原性,漂白性等性质的实验设计和现象判断,题目难度中等.

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案| A. | CO32-、Na+、H+、Cl- | B. | Ag+、NO3-、H+、Cl- | ||
| C. | Ca2+、K2+、CO${\;}_{3}^{2+}$、NO${\;}_{3}^{-}$ | D. | SO42-、K+、Na+、OH- |
 如图表示反应X (g)?4Y(g)+Z(g),在 200℃和a℃时,X的浓度随时间变化的曲线:
如图表示反应X (g)?4Y(g)+Z(g),在 200℃和a℃时,X的浓度随时间变化的曲线: (1)广州亚运会“潮流”火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.
(1)广州亚运会“潮流”火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.