��Ŀ����
����Ŀ��ʵ������ȡ�����Ļ�ѧ����ʽ��4HCl��Ũ��+MnO2 ![]() Cl2��+MnCl2+2H2O��
Cl2��+MnCl2+2H2O��
��1����Ӧ��HCl����Ԫ�صĻ��ϼ� ��
��2���ڸ�������ԭ��Ӧ�У�MnO2 ��������Ԫ�ر� �� ��HCl�ڷ�Ӧ�б��ֵ����ʰ����� ��
��3������6molCl2����ʱ����Ӧ��ת��mol���ӣ�
��4��д���÷�Ӧ�����ӷ���ʽ �� ��˫���ŷ��������ת�Ƶķ������Ŀ�� ��
���𰸡�
��1����1��
��2������,��ԭ,����,��ԭ��
��3��12
��4��4H++2Cl��+MnO2 ![]() Mn2++Cl2��+2H2O,
Mn2++Cl2��+2H2O,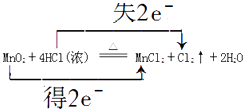
���������⣺��1����Ӧ��HCl��HΪ+1�ۣ���Ԫ�صĻ��ϼ�Ϊ��1�ۣ�
���Դ��ǣ���1�ۣ�
��2���ڸ�������ԭ��Ӧ�У�MnԪ�صĻ��ϼ۽��ͣ�MnO2 ������������Ԫ�ر���ԭ����HCl�ڷ�Ӧ�б��ֵ����ʰ������Ժͻ�ԭ�ԣ�
���Դ��ǣ���������ԭ�����ԣ���ԭ�ԣ�
��3������6molCl2����ʱ����Ӧ��ת��6mol��2����1��0��=12mol���ӣ�
���Դ��ǣ�12��
��4���÷�Ӧ�����ӷ���ʽΪ4H++2Cl��+MnO2 ![]() Mn2++Cl2��+2H2O���÷�Ӧ��ת�Ƶ�����Ϊ2e��������ת�Ʒ������ĿΪ
Mn2++Cl2��+2H2O���÷�Ӧ��ת�Ƶ�����Ϊ2e��������ת�Ʒ������ĿΪ  ��
��
���Դ��ǣ�4H++2Cl��+MnO2 ![]() Mn2++Cl2��+2H2O��
Mn2++Cl2��+2H2O��  ��
��

 �Ķ��쳵ϵ�д�
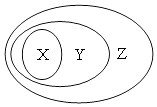
�Ķ��쳵ϵ�д�����Ŀ������ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ�в���ȷ���ǣ�������
X | Y | Z | |
A | ������ | ������ | ������ |
B | �Ȼ��� | ����� | ������ |
C | ���������� | ���������� | ������ |
D | ţ�� | ���� | ��ɢϵ |
A.A
B.B
C.C
D.D