题目内容
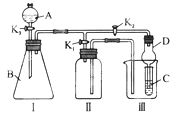
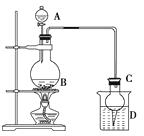
【题目】无水FeCl3呈棕红色,在空气中极易潮解100℃左右时升华,工业上常用作有机合成催化剂。某学习小组利用下图装置(夹持仪器略去)制备并收集无水FeCl3。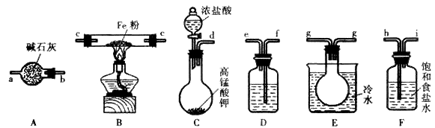
请回答:
(1)按气流方向各装置依次连接的合理顺序为(填仪器接口的字母编号)
(2)连接好各装置进行实验,实验步骤如下:检查装置气密性后,装入药品,(请按正确的顺序填入下列步骤的序号)。
①加热Fe粉反应一段时间 ②打开分液漏斗活塞通一段时间气体
③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)装置A的作用为。
(4)装置C中反应的化学方程式为。
(5)装置D中盛有的试剂为(写名称);装置E 中冷水浴的作用为。
(6)从实验安全考虑,整套装置存在一处明显不足,请指出。
【答案】
(1)dhifeccggba
(2)②①④③
(3)吸收多余的Cl2;防止外界的水蒸气进入E中
(4)2KMnO4+16HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O
(5)浓硫酸;冷凝,便于FeCl3收集
(6)B、E之间的连接导管太细,FeCl3易凝聚沉积而堵塞导管(2分)。
【解析】根据实验装置图可知,用浓盐酸与高锰酸钾溶液反应生成氯气,氯气中有氯化氢和水杂质,为制备并收集无水FeCl3 , F装置中装饱和食盐水,除去氯气中的氯化氢,D装置中装浓硫酸干燥氯气,B装置中铁与氯气反应生成氯化铁,E装置收集生成的氯化铁,实验尾气中有氯气,要用A中碱石灰吸收,由于无水FeCl3极易潮解,所以A装置还是一个干燥装置,防止吸收装置中的水份与氯化铁反应,可形成一个完整的装置,实际操作时需要先检验装置气密性,装入药品,先制一会儿氯气再加热铁粉,这样可以创造一个无氧环境,防铁被氧氧化,待反应结束后再停止加热,充分冷却得到目标产物。
(1)本套装置依次是制备氯气、除杂、反应装置、尾气处理,按照气流方向连接装置时要注意流进的导管要插入液面以下,按此原则可得连接顺序为dhifeccggba;
(2)连接好各装置进行实验,首先检查装置气密性后,然后装入药品,需要先打开分液漏斗产生一会儿氯气,再加热铁粉,反应完全后,停止加热,待充分冷却后再停止制氯气的反应,即按②①④③进行;
(3)装置A中碱石灰的作用是吸收多余的Cl2 、防止外界的水蒸气进入E中;
(4)浓盐酸和高锰酸钾混合制氯气的反应方程式为2KMnO4+ 16HCl(浓)=2KCl+2MnCl2 +5Cl2 ↑+8H2O;
(5)D装置中盛装的是浓硫酸,作用是干燥氯气;装置E是为了降温冷凝,便于FeCl3 收集;
(6)从实验安全考虑,整套装置存在一处明显不足,就是制取装置与收集装置之间连接导管太细,当温度低于于100℃时,氧化铁凝华后形成的固体可能会堵塞导管。

 阅读快车系列答案
阅读快车系列答案【题目】农科院研究员在指导农民生产的过程中发现一位农民种植的某块农田小麦产量总是比邻近地块的低。他怀疑该农田可能是缺少某种元素,为此将该块肥力均匀的农田分成面积相等的五小块,进行田间试验。除施肥不同外,其他田间处理措施相同,试验结果如下表:从表中可判断,该农田最可能缺少的元素是
地块 | 甲 | 乙 | 丙 | 丁 | 戊 |
施肥情况 | 尿素 | 磷酸二氢钾 | 磷酸二氢铵 | 硫酸铵 | 不施肥 |
小麦收获量 | 55.56 | 65.26 | 56.88 | 55.44 | 55.11 |
A.NB.K
C.PD.S