题目内容
【题目】燃料电池是符合绿色化学理念的新型发电装置。如图为氢氧燃料电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:

(1)氢氧燃料电池的能量转化主要形式是___,在导线中电子流动方向为___(用a、b表示)。
(2)负极反应式为___,正极反应式为___。
(3)用该燃料电池作电源,用Pt作电极电解饱和食盐水:
①写出阴极的电极反应式:___。
②写出总反应的离子方程式:___。
③当阳极产生7.1gCl2时,燃料电池中消耗标况下H2___L。
【答案】由化学能转变为电能 由a到b 2H2-4e-+4OH-=4H2O O2+4e-+2H2O=4OH- 2H2O+2e-=H2↑ +2OH-或2H+ +2e-=H2↑ Cl-+2H2O![]() H2↑+2OH-+Cl2↑ 2.24
H2↑+2OH-+Cl2↑ 2.24
【解析】
(1)原电池是将化学能转变为电能的装置,原电池放电时,电子从负极沿导线流向正极;(2)负极上燃料失电子发生还原反应,正极上氧气得电子生成氢氧根离子;
(3)用惰性电极电解饱和食盐水时,阳极上氯离子放电,阴极上氢离子放电;
根据转移电子守恒计算消耗氢气的物质的量
(1)该装置是把化学物质中的能量转化为电能,所以是化学能转变为电能;在原电池中,负极上失电子,正极上得电子,电子的流向是从负极流向正极,所以是 由a到b,
故答案为:由化学能转变为电能;由a到b;
(2)碱性环境中,该反应中负极上氢气失电子生成氢离子,电极反应式为2H2-4e-+4OH-=4H2O,正极上氧气得电子生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,故答案为:2H2-4e-+4OH-=4H2O;O2+4e-+2H2O=4OH-;
(3)用惰性电极电解饱和食盐水时,阴极上氢离子放电,电极反应式为:2H2O+2e-=H2↑ +2OH-或2H+ +2e-=H2↑,阳极上氯离子放电生成氯气,所以总反应离子方程式为:Cl-+2H2O![]() H2↑+2OH-+Cl2↑ ,根据转移电子守恒计算消耗氢气的物质的量,电解时,阳极上生成氯气,每生成 0.1mol 氯气转移电子的物质的量=0.1mol×(1-0)×2=0.2mol,
H2↑+2OH-+Cl2↑ ,根据转移电子守恒计算消耗氢气的物质的量,电解时,阳极上生成氯气,每生成 0.1mol 氯气转移电子的物质的量=0.1mol×(1-0)×2=0.2mol,
燃料电池中消耗氢气的物质的量=0.2mol/2=0.1mol,所以标况下体积为2.24L,
故答案为:2H2O+2e-=H2↑ +2OH-或2H+ +2e-=H2↑ ; Cl-+2H2O![]() H2↑+2OH-+Cl2↑ ; 2.24。
H2↑+2OH-+Cl2↑ ; 2.24。

【题目】乙苯是主要的化工产品。某课题组拟制备乙苯:查阅资料如下:
①几种有机物的沸点如下表:
有机物 | 苯 | 溴乙烷 | 乙苯 |
沸点/℃ | 80 | 38.4 | 136.2 |
②化学原理: ![]() +CH3CH2Br
+CH3CH2Br![]()
![]() +HBr。
+HBr。
③氯化铝易升华、易潮解。
I.制备氯化铝
甲同学选择下列装置制备氯化铝(装置不可重复使用):
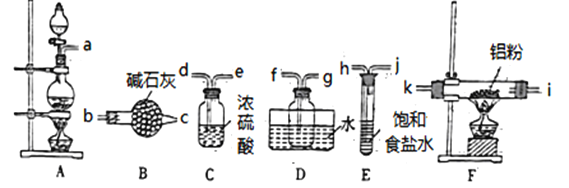
(1)本实验制备氯气的发生装置的玻璃仪器有________种。
(2)连接装置之后,检查装置的气密性,装药品。先点燃A处酒精灯,当___________ 时(填实验现象)点燃F处酒精灯。
(3)气体流动方向是从左至右,装置导管接口连接顺序a→______→k→i→f→g→_____。
(4)D装置存在明显缺陷,若不改进,导致的实验后果是______________。
II.制备乙苯
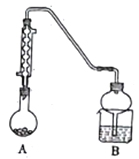
乙同学设计实验步骤如下:
步骤1:连接装置并检查气密性(如图所示,夹持装置省略)。
步骤2:用酒精灯微热烧瓶。
步骤3:在烧瓶中加入少量无水氯化铝、适量的苯和溴乙烷。
步骤4:加热,充分反应半小时。
步骤5:提纯产品。
回答下列问题:
(5)本实验加热方式宜采用_______ (填“酒精灯直接加热”或“水浴加热”)。
(6)确认本实验A中已发生了反应的试剂可以是___。
A 硝酸银溶液 B 石蕊试液
C 品红溶液 D 氢氧化钠溶液
(7)提纯产品的操作步骤有:
①过滤; ②用稀盐酸洗涤; ③少量蒸馏水水洗 ④加入大量无水氯化钙;⑤用大量水洗; ⑥蒸馏并收集136.2℃馏分 ⑦分液。
操作的先后顺序为⑤⑦__ __⑦__ __⑥(填其它代号)。
【题目】目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行了探究。已知在不同温度下的化学平衡常数(K1、K2、K3)如表所示。
化学反应 | 焓变 | 平衡 常数 | 温度/℃ | ||
500 | 700 | 800 | |||
①2H2(g)+CO(g) | ΔH1 | K1 | 2.5 | 0.34 | 0.15 |
②CO2(g)+H2(g) | ΔH2 | K2 | 1.0 | 1.70 | 2.52 |
③CO2(g)+3H2(g) | ΔH3 | K3 | |||
请回答下列问题:
(1)反应②是________(填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示);根据反应③判断ΔS________(填“>”“=”或“<”)0,在________(填“较高”或“较低”)温度下有利于反应自发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有________(填字母,后同)。
A.缩小反应容器的容积 B.增大反应容器的容积
C.升高温度 D.使用合适的催化剂 E.从平衡体系中及时分离出CH3OH
(4)500 ℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1 mol·L-1、0.8 mol·L-1、0.3 mol·L-1、0.15 mol·L-1,则此时v(正)________v(逆)(填“>”“=”或“<”)。