题目内容
某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源,减少大气污染.已知制酒的方法有三种:
①在催化剂作用下乙烯与水反应
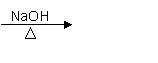
②CH3CH2Br+H2O
CH3CH2OH+HBr
③(C6H10O5)n(淀粉)+nH2O
nC6H12O6(葡萄糖)
C6H10O6(葡萄糖)
2C2H5OH+2CO2↑
(1)方法①反应的化学方程式是
(2)为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?请简述理由
(3)如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是
A.①B.③C.①③D.①②③
①在催化剂作用下乙烯与水反应
②CH3CH2Br+H2O
| ||
| △ |
③(C6H10O5)n(淀粉)+nH2O
| 淀粉酶 |
C6H10O6(葡萄糖)
| 酒化酶 |
(1)方法①反应的化学方程式是
CH2=CH2+H2O
CH3CH2OH
| 催化剂 |
CH2=CH2+H2O
CH3CH2OH
.反应类型为| 催化剂 |
加成反应
加成反应
,方法②的化学反应类型是取代反应
取代反应
.(2)为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?请简述理由
方法③;淀粉是绿色植物光合作用的产物,可循环利用
方法③;淀粉是绿色植物光合作用的产物,可循环利用
.(3)如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是
A
A
(填序号)A.①B.③C.①③D.①②③
分析:(1)根据乙烯的性质以及加成反应和取代反应的特点来回答;
(2)根据三种实验方案来回答;
(3)在有机反应中,加成反应原子利用率是100%.
(2)根据三种实验方案来回答;
(3)在有机反应中,加成反应原子利用率是100%.
解答:解:(1)加成反应的特点是“有去无回”和取代反应的特点是“有去有回”,乙醇和水之间发生的是加成反应,方程式为:CH2=CH2+H2O
CH3CH2OH,反应CH3CH2Br+H2O
CH3CH2OH+HBr中,溴原子被羟基取代,属于取代反应,故答案为:CH2=CH2+H2O
CH3CH2OH;加成反应;取代反应;
(2)因为淀粉是可再生资源,不符合要求,而乙烯,溴乙烷都是来自于以石油为原料制得的产品,是不可再生资源,利用它们制成酒精还不如直接利用石油,不符合要求,方法③淀粉是绿色植物光合作用的产物,可循环利用,所以是运用了方法③,故答案为:方法③;淀粉是绿色植物光合作用的产物,可循环利用;
(3)加成反应原子利用率是100%,符合绿色化学的思想,故A正确,故答案为:A.
| 催化剂 |
| ||
| △ |
| 催化剂 |
(2)因为淀粉是可再生资源,不符合要求,而乙烯,溴乙烷都是来自于以石油为原料制得的产品,是不可再生资源,利用它们制成酒精还不如直接利用石油,不符合要求,方法③淀粉是绿色植物光合作用的产物,可循环利用,所以是运用了方法③,故答案为:方法③;淀粉是绿色植物光合作用的产物,可循环利用;
(3)加成反应原子利用率是100%,符合绿色化学的思想,故A正确,故答案为:A.
点评:本题是一道化学和实际生产结合的题目,注意利用常见的有机化学反应类型及有机物的性质来解答,考查角度广,难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
 ①在催化剂作用下乙烯与水反应
①在催化剂作用下乙烯与水反应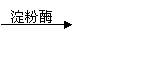 ③(C6H10O5)n(淀粉)+nH2O nC6H12O6(葡萄糖)
③(C6H10O5)n(淀粉)+nH2O nC6H12O6(葡萄糖)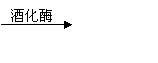
 CH3CH2OH+HBr
CH3CH2OH+HBr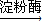 nC6H12O6(葡萄糖)
nC6H12O6(葡萄糖)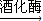 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑