题目内容
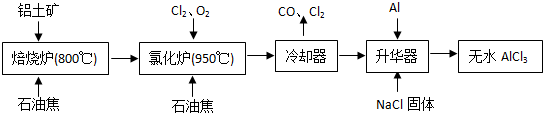
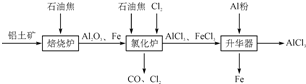
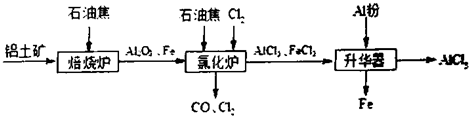
工业上由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备无水AlCl3.的流程如下
已知:AlCl3,FeCl3,分别在183℃、315℃升华
(1)在焙烧炉中发生反应:
①Fe2O3(S)+3C(s)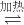 2Fe(s)+3CO(g)△H=-492.7kJ?mol-1
2Fe(s)+3CO(g)△H=-492.7kJ?mol-1
②3CO(g)+Fe2O3(s)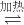 2Fe(s)+3CO2(g)△H=+25.2kJ?mol-1
2Fe(s)+3CO2(g)△H=+25.2kJ?mol-1
③反应2Fe2O3(s)+3C(s)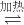 4Fe(s)+3CO2(g)△H=______kJ?mol-1
4Fe(s)+3CO2(g)△H=______kJ?mol-1
(2)①Al2O3,Cl2和C在氯化炉中高温下发生反应,当生成1molAlCl3.时转移______ mol电子;炉气中含有大量CO和少量Cl2,可用Na2SO3.溶液除去Cl2,其离子方程式为:______.在温度约为700℃向升华器中加入铝粉,发生反应的化学方程式为______.充分反应后温度降至______以下(填“183℃、315℃之一),开始分离收集AlCl3.
②将AlCl3?6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的______(填字母序号).
①氧化性 ②吸水性 ③难挥发性 ④脱水性
a.只有①b.只有②c.只有②③d.只有②③④
(3)海洋灯塔电池是利用铝、石墨为电极材料,海水为电解质溶液,构成电池的其正极反应式______;与铅蓄电池相比.释放相同电量时,所消耗金属电极材料的质量比m(A1):m(Pb)=______.
解:(1)已知:①Fe2O3(S)+3C(s)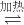 2Fe(s)+3CO(g)△H=-492.7kJ?mol-1
2Fe(s)+3CO(g)△H=-492.7kJ?mol-1
②3CO(g)+Fe2O3(s)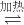 2Fe(s)+3CO2(g)△H=+25.2kJ?mol-1
2Fe(s)+3CO2(g)△H=+25.2kJ?mol-1
由盖斯定律,①+②得:2Fe2O3(s)+3C(s)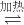 4Fe(s)+3CO2(g);故△H=(-492.7kJ/mol)+25.2kJ/mol=-467.5kJ/mol;
4Fe(s)+3CO2(g);故△H=(-492.7kJ/mol)+25.2kJ/mol=-467.5kJ/mol;
故答案为:-467.5;
(2)①、根据工艺流程可知氯化炉的产物,经冷却、升华可制备无水AlCl3,说明氯化炉的产物中含有A1C13,冷凝器尾气含有CO,所以Al2O3、C12和C反应,生成A1C13和CO,反应方程式为A12O3+3C12+3C 2A1C13+3CO,反应中氯元素化合价由0价降低为-1价,氯气是氧化剂,故生成1mol AlCl3时转移电子为1mol×3=3mol,
2A1C13+3CO,反应中氯元素化合价由0价降低为-1价,氯气是氧化剂,故生成1mol AlCl3时转移电子为1mol×3=3mol,
Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为C1-,反应离子方程式为SO32-+C12+H2O═SO42-+2C1-+2H+,
由工艺流程可知,升华器中主要含有AlCl3和FeCl3,加入少量Al除去FeCl3,Al与FeCl3反应生成Fe、AlCl3,反应方程式为Al+FeCl3 AlCl3+Fe,
AlCl3+Fe,
由题目信息可知,AlCl3的升华温度更低,应控制温度使AlCl3升华,且FeCl3不升华,故温度应控制在315℃以下,
故答案为:3;SO32-+C12+H2O═SO42-+2C1-+2H+;Al+FeCl3 AlCl3+Fe;315℃;
AlCl3+Fe;315℃;
②AlCl3的水解,直接加热AlCl3?6H2O,水解彻底生成氢氧化铝,得不到氯化铝,浓硫酸吸水,同时可以生成HCl抑制氯化铝水解,利用浓硫酸的吸水性与难挥发性,
故答案为:c;
(3)该原电池实质是金属铝发生的吸氧腐蚀,氧气在正极放电生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,
电量相同,则原电池转移电子相同,令转移电子为3mol,则n(Al)= =1mol、n(Pb)=
=1mol、n(Pb)= =1.5mol,故m(A1):m(Pb)=1mol×27g/mol:1.5mol×207g/mol=2:23
=1.5mol,故m(A1):m(Pb)=1mol×27g/mol:1.5mol×207g/mol=2:23
故答案为:O2+4e-+2H2O=4OH-;2:23.
分析:(1)由盖斯定律定律,①+②得:2Fe2O3(s)+3C(s)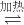 4Fe(s)+3CO2(g);反应热也进行相应的计算;
4Fe(s)+3CO2(g);反应热也进行相应的计算;
(2)①根据工艺流程可知升华器中含有AlCl3等,所以Al2O3、C12和C反应会生成A1C13,由冷凝器尾气可知还会生成CO,根据氯元素化合价变化计算注意电子数目;
Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为C1-;
由工艺流程可知,升华器中主要含有AlCl3和FeCl3,加入少量Al除去FeCl3,Al与FeCl3反应生成Fe、AlCl3;
由题目信息可知,AlCl3的升华温度更低,应控制温度使AlCl3升华,且FeCl3不升华;
②AlCl3的水解,直接加热AlCl3?6H2O,水解彻底生成氢氧化铝,得不到氯化铝,浓硫酸吸水,同时可以生成HCl抑制氯化铝水解;
(3)该原电池实质是金属铝发生的吸氧腐蚀,氧气在正极放电生成氢氧根离子;
电量相同,则原电池转移电子相同,令转移电子为3mol,根据元素化合价计算n(Al)、n(Pb),再根据m=nM计算.
点评:本题考查反应热的计算、对工艺流程的理解与条件控制、盐类水解、原电池、化学计算等,难度中等,理解工艺流程是解题的关键,是对学生综合能力的考查,需要学生具备扎实的基础,对学生的分析问题、解决问题的能力有较高要求.
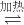 2Fe(s)+3CO(g)△H=-492.7kJ?mol-1
2Fe(s)+3CO(g)△H=-492.7kJ?mol-1②3CO(g)+Fe2O3(s)
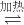 2Fe(s)+3CO2(g)△H=+25.2kJ?mol-1
2Fe(s)+3CO2(g)△H=+25.2kJ?mol-1由盖斯定律,①+②得:2Fe2O3(s)+3C(s)
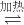 4Fe(s)+3CO2(g);故△H=(-492.7kJ/mol)+25.2kJ/mol=-467.5kJ/mol;
4Fe(s)+3CO2(g);故△H=(-492.7kJ/mol)+25.2kJ/mol=-467.5kJ/mol;故答案为:-467.5;
(2)①、根据工艺流程可知氯化炉的产物,经冷却、升华可制备无水AlCl3,说明氯化炉的产物中含有A1C13,冷凝器尾气含有CO,所以Al2O3、C12和C反应,生成A1C13和CO,反应方程式为A12O3+3C12+3C
 2A1C13+3CO,反应中氯元素化合价由0价降低为-1价,氯气是氧化剂,故生成1mol AlCl3时转移电子为1mol×3=3mol,
2A1C13+3CO,反应中氯元素化合价由0价降低为-1价,氯气是氧化剂,故生成1mol AlCl3时转移电子为1mol×3=3mol,Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为C1-,反应离子方程式为SO32-+C12+H2O═SO42-+2C1-+2H+,
由工艺流程可知,升华器中主要含有AlCl3和FeCl3,加入少量Al除去FeCl3,Al与FeCl3反应生成Fe、AlCl3,反应方程式为Al+FeCl3
 AlCl3+Fe,
AlCl3+Fe,由题目信息可知,AlCl3的升华温度更低,应控制温度使AlCl3升华,且FeCl3不升华,故温度应控制在315℃以下,
故答案为:3;SO32-+C12+H2O═SO42-+2C1-+2H+;Al+FeCl3
 AlCl3+Fe;315℃;
AlCl3+Fe;315℃;②AlCl3的水解,直接加热AlCl3?6H2O,水解彻底生成氢氧化铝,得不到氯化铝,浓硫酸吸水,同时可以生成HCl抑制氯化铝水解,利用浓硫酸的吸水性与难挥发性,
故答案为:c;
(3)该原电池实质是金属铝发生的吸氧腐蚀,氧气在正极放电生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,
电量相同,则原电池转移电子相同,令转移电子为3mol,则n(Al)=
 =1mol、n(Pb)=
=1mol、n(Pb)= =1.5mol,故m(A1):m(Pb)=1mol×27g/mol:1.5mol×207g/mol=2:23
=1.5mol,故m(A1):m(Pb)=1mol×27g/mol:1.5mol×207g/mol=2:23故答案为:O2+4e-+2H2O=4OH-;2:23.
分析:(1)由盖斯定律定律,①+②得:2Fe2O3(s)+3C(s)
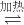 4Fe(s)+3CO2(g);反应热也进行相应的计算;
4Fe(s)+3CO2(g);反应热也进行相应的计算;(2)①根据工艺流程可知升华器中含有AlCl3等,所以Al2O3、C12和C反应会生成A1C13,由冷凝器尾气可知还会生成CO,根据氯元素化合价变化计算注意电子数目;
Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为C1-;
由工艺流程可知,升华器中主要含有AlCl3和FeCl3,加入少量Al除去FeCl3,Al与FeCl3反应生成Fe、AlCl3;
由题目信息可知,AlCl3的升华温度更低,应控制温度使AlCl3升华,且FeCl3不升华;
②AlCl3的水解,直接加热AlCl3?6H2O,水解彻底生成氢氧化铝,得不到氯化铝,浓硫酸吸水,同时可以生成HCl抑制氯化铝水解;
(3)该原电池实质是金属铝发生的吸氧腐蚀,氧气在正极放电生成氢氧根离子;
电量相同,则原电池转移电子相同,令转移电子为3mol,根据元素化合价计算n(Al)、n(Pb),再根据m=nM计算.
点评:本题考查反应热的计算、对工艺流程的理解与条件控制、盐类水解、原电池、化学计算等,难度中等,理解工艺流程是解题的关键,是对学生综合能力的考查,需要学生具备扎实的基础,对学生的分析问题、解决问题的能力有较高要求.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目