题目内容
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
① 若为NH4Cl 溶液,则四种离子浓度的由大到小的顺序是___________。(填序号)
② 若为HCl 和NH4Cl 混合溶液,则四种离子浓度的由大到小的顺序是_________;
若为NH3· H2O 和NH4Cl 混合溶液,四种离子浓度的由大到小的顺序是__________。
③ 若该溶液是由体积相等的HCl溶液和氨水混合而成,且恰好呈中性,则混合前c(HCl) _____c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(OH-)____c(NH4+)。
| A.c(NH4+)>c(Cl-)>c(OH-)>c(H+) | B.c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D.c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
② 若为HCl 和NH4Cl 混合溶液,则四种离子浓度的由大到小的顺序是_________;
若为NH3· H2O 和NH4Cl 混合溶液,四种离子浓度的由大到小的顺序是__________。
③ 若该溶液是由体积相等的HCl溶液和氨水混合而成,且恰好呈中性,则混合前c(HCl) _____c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(OH-)____c(NH4+)。
(1)C (2)B; A (3) <; <
试题分析:① 若为NH4Cl 溶液,由于NH4+水解消耗水电离产生的OH-离子,所以这四种离子浓度的由大到小的顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-)。选项为:C。② 由于溶液中的Cl-由HCl 和NH4Cl共同电离产生,所以,溶液中的H+有酸的电离、NH4+的水解产生,所以c(H+)>c(NH4+);盐水解的程度很微弱,故c(NH4+)>c(OH-)。因此在HCl 和NH4Cl 混合溶液中四种离子浓度的由大到小的顺序是c(Cl-)>c(H+)>c(NH4+)>c(OH-)。选项为:B。若为NH3· H2O 和NH4Cl 混合溶液,由于NH3· H2O的电离作用大于NH4+水解作用。C(NH4+)>c(Cl-),c(OH-)>c(H+)。盐的电离远大于水的电离,所以c(Cl-) >c(OH-)。故再此混合溶液,四种离子浓度的由大到小的顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+)。选项为:A.③ 若该溶液是由体积相等的HCl溶液和氨水混合而成,且恰好呈中性,则c(NH4+)=c(Cl-),c(OH-)=c(H+)。由于HCl为强酸,完全电离,NH3·H2O为弱碱,部分电离,所以要保证混合后溶液呈中性,n(NH3·H2O) >n(HCl).即混合前c(HCl) <c(NH3·H2O)。混合后溶液中盐电离产生的NH4+比水电离产生的OH-物质的量要多。故c(OH-) <c(NH4+)。

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
 H++B2-。回答下列问题。
H++B2-。回答下列问题。

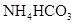


 HCO3-+OH- 热的纯碱溶液清洗油污
HCO3-+OH- 热的纯碱溶液清洗油污 Al(OH)3(胶体)+3H+ 明矾净水
Al(OH)3(胶体)+3H+ 明矾净水 CH3COO- + H3O+
CH3COO- + H3O+