题目内容
【题目】按要求填空:有下列物质:①O2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩N2,回答下列问题:
(1)只含有极性键的是________;只含有非极性键的是________;含有极性键和非极性键的是________;只含有离子键的离子化合物是________;含有非极性键的离子化合物是________;
(2)写出⑤、⑧、⑨的电子式_____________、______________、________________;
(3)溶于水只破坏离子键的是__________;溶于水既破坏离子键又破坏共价键的是________________;
【答案】②③ ①⑩ ⑧ ④⑦ ⑤ ![]()
![]()
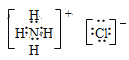 ④⑥⑦⑨ ⑤
④⑥⑦⑨ ⑤
【解析】
(1)一般来说,活泼金属和活泼非金属元素之间易形成离子键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键,含有离子键的化合物是离子化合物,只含共价键的化合物是共价化合物。
(2)⑤、⑧、⑨的电子式![]() 、
、![]() 、
、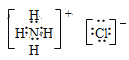 ;
;
(3)未破坏化学键说明没有发生化学反应或没有电解质熔融或溶于水,物质发生物理变化;仅离子键被破坏说明离子化合物溶于水或熔融或发生化学反应离子键被破坏;仅共价键被破坏说明共价化合物溶于水或发生化学反应;离子键和共价键同时被破坏说明该物质发生化学反应。
(1)①O2⑩N2中只含非极性键,属于单质;
②CO2 ③NH3中只含极性键,属于共价化合物;
⑧H2O2 含有H-O极性键和O-O非极性键,属于共价化合物;
⑤Na2O2中含有离子键和非极性键,属于离子化合物;
⑥NaOH、⑨NH4Cl中含有离子键和极性键,属于离子化合物;
⑦CaBr2、④Na2O中只含离子键,属于离子化合物;
只含极性键的是②③;
只含非极性键的是①⑩ ;
含有极性键和非极性键的是⑧;
只含有离子键的离子化合物是④⑦;
含有非极性键的离子化合物是⑤.
(2)⑤、⑧、⑨的电子式分别为:![]() 、
、![]() 、
、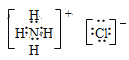 ;
;
(3)离子化合物溶于水时,离子键被破坏;含有共价键的离子化合物溶于水时,其共价键也有可能被破坏。
④Na2O溶于水时与水反应生成氢氧化钠,离子键被破坏; ⑥NaOH 、 ⑦CaBr2 、⑨NH4Cl溶于水电离出其对应的阴、阳离子,故溶于水只破坏离子键的是④⑥⑦⑨;
氧化钠与水反应生成氢氧化钠和氧气,故溶于水时既破坏了离子键又破坏了共价键是⑤。

 阅读快车系列答案
阅读快车系列答案【题目】下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白(填写序号不得分):
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:__________。(填元素符号)
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是__________,碱性最强的化合物的化学式是__________________。
(3)比较①与⑤的最高价氧化物对应的水化物,________________的酸性强(填化学式)
(4)工业上制取②的氢化物的化学方程式_______________________________________;
②的氢化物与②的最高价氧化物的水化物反应所得的产物化学式为_____________。
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因________________________________________________(用化学方程式表示)
(6)比较③与⑥的氢化物,_______________更稳定,__________沸点更高(填化学式)
(7)写出④的单质与水反应的化学方程式_________________________________________。
(8)写出⑦元素的离子结构示意图______________________,该离子半径_________S2-(填“﹥”或“﹤”)写出⑩元素在周期表的位置__________________________。