题目内容
已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2 充入1L的密闭容器中发生反应,测得有关数据如下表:
充入1L的密闭容器中发生反应,测得有关数据如下表:
实验 编号 | 温度 | 时间 min 物质 的量mol | 0 | 10 | 20 | 40 | 50 |
1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
(1)开展实验1和实验2的目的是: 。
(2)180℃、反应到40min时,体系 (填“达到”或“未达到”)平衡状态,理由是: ;此时CH4的平衡转化率为: 。
(3)在一定条件下,反应时间t与转化率μ(NO2)的关系如图所示,请在图像中画出180℃时,压强为P2(设压强P2>P1)的变化曲线,并做必要的标注。
练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
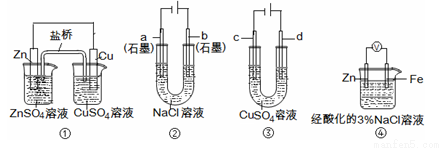
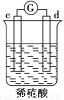
有a、b、c、d四个金属电极,有关的化学装置、部分反应现象如下:
实验装置 |
|
|
|
|
实验现象 | a极质量减小, b极质量增加 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是
A.a>b>c>d B.b>c>d>a C.a>b>d>c D.d>a>b>c
下列生活中常见的现象中,其反应原理不涉及氧化还原反应的是
A.铁的冶炼 | B.电池放电 | C.碳酸氢钠作发酵粉 | D.天然气燃烧 |
|
|
|
|