题目内容
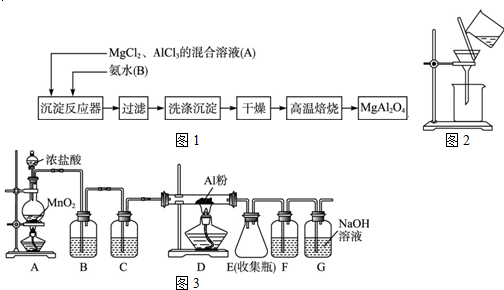
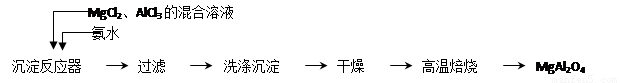
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下:


(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式????????????? 。
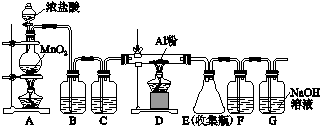
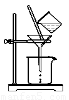
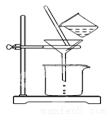
(2)如图所示,过滤操作中的一处错误是????????????? ?? 。

判断流程中沉淀是否洗净所用的试剂是??????????? 。高温焙烧时,用于盛放固?? 体的仪器名称是??????????? 。
(3)在25℃下,向浓度均为0.01 mol?L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成_________________沉淀(填化学式),生成该沉淀的离子方程式_____________________(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10 -34。)
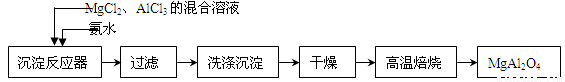
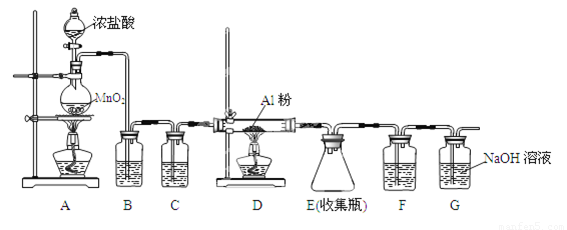
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
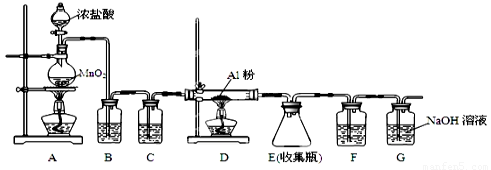
装置B中盛放饱和NaCl溶液,该装置的主要作用是????????? ;F中试剂的作用是???????? ;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为??????????????????? 。
(5)将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为??????????????????????? g。
(1)2 Al(OH)3+Mg (OH)2 = MgAl2O4? + 4H2O (2分)??
(2)漏斗下端尖嘴未紧贴烧杯内壁(1分)??? AgNO3溶液(或硝酸酸化的AgNO3溶液)(1分);坩埚(1分)
(3)Al(OH)3(2分)???????? Al3++ 3NH3·H2O=Al(OH)3+ 3NH4+(2分)
(4)除去HCl(1分);吸收水蒸气(1分);碱石灰(或NaOH与CaO混合物)(1分)
(5)8.00(2分)
【解析】
试题分析:(1) MgCl2、AlCl3的混合溶液中加入过量氨水,过滤所得沉淀为Al(OH)3和Mg (OH)2 ,故反应为: 2Al(OH)3+Mg (OH)2 = MgAl2O4 + 4H2O (2) 过滤操作注意:一贴、二低、三靠。漏斗下端尖嘴要紧贴烧杯内壁。根据反应流程,沉淀中应该附着氯离子和铵根离子,若判断是否洗净,可以取少量最后一次洗涤液,加入AgNO3溶液(或硝酸酸性的AgNO3溶液)溶液进行判断,若生成白色沉淀,则说明没有洗涤干净;若没有沉淀生成,则说明已经洗涤干净。高温焙烧固体应在坩埚中进行。(3) 根据溶度积计算可知,形成Al(OH)3沉淀所需氢氧根离子浓度最小,故先生成Al(OH)3沉淀,一水合氨是弱碱,书写离子方程式不能拆开,且生成沉淀不再溶解,离子方程式为:Al3++ 3NH3·H2O=Al(OH)3+ 3NH4+。(4) B中的饱和食盐水是为了除去混有的HCl气体;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以可以加入碱石灰来代替F和G的作用。(5)设Mg和Cu的物质的量分别为amol、bmol,根据电子守恒可得:2a+2b=0.08×3→a+b=0.12,沉淀的质量=金属质量+氢氧根质量=3.92+0.12×2×17=8.00
考点:考查制备实验方案的设计;镁、铝的重要化合物。

 阅读快车系列答案
阅读快车系列答案