题目内容
【题目】用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)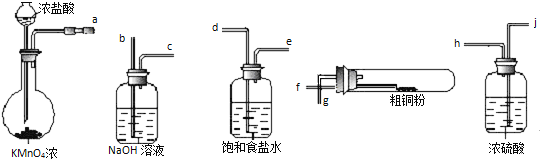
①按气流方向连接各仪器接口顺序是:![]() ______ .
______ .
②反应时,盛粗铜粉的试管中的现象是 ______ .
③已知:氯化铜溶液中有如下转化关系:
![]()
![]()
蓝色 绿色
该同学取氯化铜晶体配成蓝绿色溶液Y,进行如下实验,其中能证明溶液中有上述转化关系的是 ______ ![]() 填序号
填序号![]() .
.
A.将Y稀释,发现溶液呈蓝色
B.在Y中加入![]() 晶体,溶液变为绿色
晶体,溶液变为绿色
C.在Y中加入NaCl固体,溶液变为绿色
D.取Y进行电解,溶液颜色最终消失.
【答案】![]() 铜粉逐渐减少并生成大量棕黄色的烟 ABC
铜粉逐渐减少并生成大量棕黄色的烟 ABC
【解析】
![]() 要制备收集纯净的氯气应该除去氯气中的杂质
要制备收集纯净的氯气应该除去氯气中的杂质![]() 水、
水、![]() ,除氯化氢用饱和食盐水,除去水用浓硫酸,然后与铜反应,最后尾气处理用氢氧化钠,据此解答;
,除氯化氢用饱和食盐水,除去水用浓硫酸,然后与铜反应,最后尾气处理用氢氧化钠,据此解答;
![]() 粗铜粉与氯气反应生成棕黄色的氯化铜;
粗铜粉与氯气反应生成棕黄色的氯化铜;
![]() 根据勒夏特列原理,通过改变浓度使平衡发生移动从而使溶液颜色发生改变,即可证明溶液中有
根据勒夏特列原理,通过改变浓度使平衡发生移动从而使溶液颜色发生改变,即可证明溶液中有![]()
![]() 的转化关系。
的转化关系。
![]() 从a出来的气体含有氯化氢和水蒸气,依次通过dejh除去氯化氢和水蒸气,然后与铜反应,最后尾气处理用氢氧化钠,则依次再通过fgbc,所以按照气流方向各仪器接口的连接顺序为
从a出来的气体含有氯化氢和水蒸气,依次通过dejh除去氯化氢和水蒸气,然后与铜反应,最后尾气处理用氢氧化钠,则依次再通过fgbc,所以按照气流方向各仪器接口的连接顺序为![]() ,故答案为:
,故答案为:![]() ;
;
![]() 粗铜粉与氯气反应的现象为:铜粉逐渐减少并生成大量棕黄色的烟,故答案为:铜粉逐渐减少并生成大量棕黄色的烟;
粗铜粉与氯气反应的现象为:铜粉逐渐减少并生成大量棕黄色的烟,故答案为:铜粉逐渐减少并生成大量棕黄色的烟;
![]() 将Y稀释,平衡向左移动,溶液呈蓝色,可以能够证明
将Y稀释,平衡向左移动,溶液呈蓝色,可以能够证明![]() 溶液中转化关系,故A正确;
溶液中转化关系,故A正确;
B.在Y中加入![]() 晶体,溶液中
晶体,溶液中![]() 浓度增大,平衡向右移动,溶液变为绿色,可以能够证明
浓度增大,平衡向右移动,溶液变为绿色,可以能够证明![]() 溶液中转化关系,故B正确;
溶液中转化关系,故B正确;
C.在Y中加入NaCl固体,溶液中氯离子浓度增大,平衡向右移动,溶液变为绿色,可以能够证明![]() 溶液中转化关系,故C正确;
溶液中转化关系,故C正确;
D.取Y进行电解,铜离子放电,溶液颜色最终消失,不能可以能够证明![]() 溶液中转化关系,故D错误。
溶液中转化关系,故D错误。
故答案为:ABC。

【题目】不同温度下,三个体积均为1L的密闭容器中发生反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H=-867 kJ.mol-1,实验测得起始、平衡时的有关数据如表。下列说法正确的是
N2(g)+CO2(g)+2H2O(g) △H=-867 kJ.mol-1,实验测得起始、平衡时的有关数据如表。下列说法正确的是
容器编号 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | ||||
CH4 | NO2 | N2 | CO2 | H2O | NO2 | ||
I | T1 | 0.50 | 1.2 | 0 | 0 | 0 | 0.40 |
II | T2 | 0.30 | 0.80 | 0.20 | 0.20 | 0.40 | 0.60 |
III | T3 | 0.40 | 0.70 | 0.70 | 0.70 | 1.0 | |
A.T1<T2
B.若升高温度,正反应速率减小,逆反应速率增大,平衡逆移
C.平衡时,容器I中反应放出的热量为693.6 kJ
D.容器III中反应起始时v 正(CH4) <v逆(CH4)