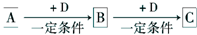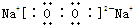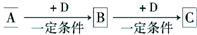��Ŀ����
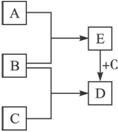
��֪A��B��C�ǵ�2���ڵķǽ���Ԫ�أ���ԭ��������������������֮������γ�AC��BC�Լ�AC2��BC2���ӣ�DԪ����һ�ֶ�����Ԫ�أ�����A��B��C�ɷֱ��γɵ���������ȵ����ַ��ӡ������:
��1��д��A��B��C��D��Ӧ��Ԫ�ط��ţ�A��______��B�� _____��C��______��D��______��
��2��д����ҵ������BD3��������Ӧ�Ļ�ѧ����ʽ��__________________________��
![]() ��3������ΪB��C��DԪ���γɵĻ�����֮��_________����ܡ����ܡ�����������ķ�ӦBC+BD3 D BC2+D2C���ó�������۵�������________________��
��3������ΪB��C��DԪ���γɵĻ�����֮��_________����ܡ����ܡ�����������ķ�ӦBC+BD3 D BC2+D2C���ó�������۵�������________________��
![]() ��4�����º�ѹ��,��һ����ɱ���ܱ������з������з�Ӧ��
��4�����º�ѹ��,��һ����ɱ���ܱ������з������з�Ӧ��
4AC��g��+2BC2��g�� 4AC2��g��+B2��g���������������£��������г���AC��BC2��1 mol��ƽ��ʱ������AC2��B2��a mol,��AC��ת������__________���ú�a�Ĵ���ʽ��ʾ����
����ά���¶Ȳ���,��һ�����Ӧǰ����ʼ�����ͬ�ݻ��̶����ܱ������з������������Ļ�ѧ��Ӧ,��ʼʱ���������г���AC��BC2��1 mol,��ƽ��ʱ����AC2��B2��b mol,��b����е�a���бȽ�,��a_________b���������������=������ȷ��������
��1��C N O H
��2��4NH3+5O2![]() 4NO+5H2O
4NO+5H2O
��3������ �ڴ˷�Ӧ��ϵ�У�ֻ��ʧ���ӵ����ʣ�û�еõ��ӵ�����
��4����80a% ��
����:
������Ԫ�ػ����Pƽ����ۺ��⣬�漰��֪ʶ��Ͽ�������ѧ�����ۺ�����������˼·���£�A��B��C�ǵ�2���ڵķǽ���Ԫ�أ���ԭ����������������һ��ͻ�ƿڣ�DԪ����һ�ֶ�����Ԫ�أ�����A��B��C�ɷֱ��γɵ���������ȵ����ַ�������һ��ͻ�ƿڣ����ȵ����壬�ټ��������ߵķ���ʽ�����Կ�֪A��C��B��N��C��O��D��H��
��2��NH3�Ĵ�����ԭ����4NH3+5O2![]() 4NO+5H2O
4NO+5H2O
��3��������ԭ��Ӧ���ص�ʧ�����غ��ԭ�����е���ʧ��������ʽֻ��ʧ���ӵ����ʣ�û�еõ��ӵ����ʣ����Բ��ܷ�����
��4���÷�Ӧ��4CO+2NO2====4CO2+N2,�������֪CO2Ϊ4a/5 mol, N2Ϊa/5 mol������ת����COΪ4a/5 mol,��ת����Ϊ80a�����������г���AC��BC2��1 mol,�ݻ������ͬ�ҹ̶��������º��ݣ���Ӧ����������У�����ѹǿ��С�����º��º�ѹ�µ�ѹǿ���ں��º���ʱ��ѹǿ�����Ժ��º�ѹ�·�Ӧ����������г̶ȴ�����a��b��