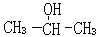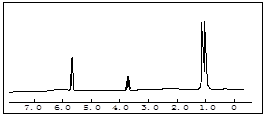题目内容
(5分)某有机物的质量为3.0g,完全燃烧后产物通过浓H2SO4,浓H2SO4质量增加3.6g;其余的气体再通过碱石灰,被完全吸收,碱石灰质量增加6.6g。已知该有机物的蒸气对氢气的相对密度是30。
(1)求该有机物的分子式。(要求写计算过程)
(2)若该有机物能与金属钠反应,经催化氧化后的生成物含有醛基(-CHO),请写出该有机物的结构简式,并对它进行命名。
(1)求该有机物的分子式。(要求写计算过程)
(2)若该有机物能与金属钠反应,经催化氧化后的生成物含有醛基(-CHO),请写出该有机物的结构简式,并对它进行命名。
(1)化合物的蒸气对氢气的相对密度是30
所以该有机物的相对分子质量是30×2=60
因此3.0 g有机物A的物质的量是0.05mol
浓硫酸增重3.6g,说明生成物水是3.6g,物质的量是
碱石灰增重6.6g,说明CO2的质量是6.6g,其物质的量是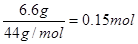 、
、
所以根据原子守恒可知有机物中碳、氢原子的个数分别是3和8
因此氧原子的个数是
所以有机物的分子式为C3H8O。
(2)根据有机物的化学性质可判断,该有机物是醇类。氧化产物含有醛基,所以是1-丙醇,结构简式为CH3CH2CH2OH
所以该有机物的相对分子质量是30×2=60
因此3.0 g有机物A的物质的量是0.05mol
浓硫酸增重3.6g,说明生成物水是3.6g,物质的量是

碱石灰增重6.6g,说明CO2的质量是6.6g,其物质的量是
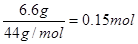 、
、所以根据原子守恒可知有机物中碳、氢原子的个数分别是3和8
因此氧原子的个数是

所以有机物的分子式为C3H8O。
(2)根据有机物的化学性质可判断,该有机物是醇类。氧化产物含有醛基,所以是1-丙醇,结构简式为CH3CH2CH2OH
考查有机物分子式及结构简式的确定。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
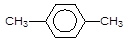 对二甲苯
对二甲苯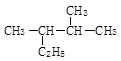 ______________ _
______________ _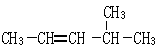 __________________ _
__________________ _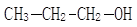 2-丙醇:
2-丙醇: