题目内容
氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量。在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ。下列关系式中正确的是
| A.Q1+ Q2<2Q3 | B.Q1+ Q2>2Q3 |
| C.Q1+ Q2<Q3 | D.Q1+ Q2>Q3 |
A
本题从微观的角度考查反应热的计算。在化学反应中,断键需要吸热,而形成新的化学键时则会放出能量。氢气在氯气中燃烧属于放热反应,化学方程式为:
 所以反应中放出的能量为:2Q3-Q1+ Q2,因此Q1+ Q2< 2Q3,即选项A符合题意。
所以反应中放出的能量为:2Q3-Q1+ Q2,因此Q1+ Q2< 2Q3,即选项A符合题意。
练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
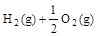 =H2O(g) △H1=a kJ
=H2O(g) △H1=a kJ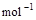 , ②
, ②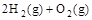 =2H2O(g)△H2=b kJ
=2H2O(g)△H2=b kJ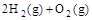 =2H2O(l)
=2H2O(l)  CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1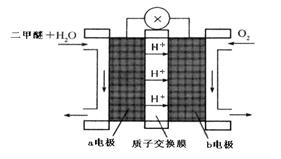
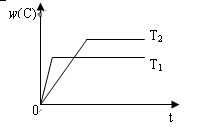
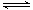 2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是( )
2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是( )