题目内容
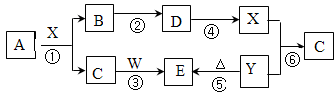
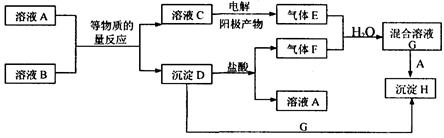
(10分)A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。

(1)X的单质与A反应的化学方程式是 。
(2)若试剂1是NaOH溶液。X的单质与试剂1反应的离子方程式是
。
(3)若试剂1和试剂2均是稀硫酸。
①将物质C溶于水,其溶液呈 性(填“酸”、“碱”或“中”)。
②某高效净水剂是由Y(OH)SO4聚合得到的,工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式为 。

(1)X的单质与A反应的化学方程式是 。
(2)若试剂1是NaOH溶液。X的单质与试剂1反应的离子方程式是
。
(3)若试剂1和试剂2均是稀硫酸。
①将物质C溶于水,其溶液呈 性(填“酸”、“碱”或“中”)。
②某高效净水剂是由Y(OH)SO4聚合得到的,工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式为 。
(1)2Al+Fe2O3
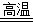 Al2O3+2Fe
Al2O3+2Fe(2)2Al+2OH-+2H2O=2AlO2-+3H2↑
(3)①酸 ②2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑
试题分析:首先观察X和A反应生成B和Y,X、Y是常见金属,而A、B是氧化物,那么此反应就是铝热反应。则X是铝,A氧化铁。所以(1)的方程式可以写出来。(2)若试剂1是氢氧化钠,此反应则为铝和氢氧化钠反应生成偏铝酸钠和氢气、水的反应。(3)①若试剂1是稀硫酸,铝和稀硫酸反应生成C为硫酸铝,溶液呈酸性,因为C为强酸弱碱盐,发生水解显酸性。②E为硫酸亚铁,根据元素守恒,则反应还生成了硫酸钠,配平方程式即可。
点评:本题抓住关键反应进行推断,后面的填空题目不难,只要推断出X、Y是什么金属便可以轻松解答。

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目