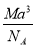题目内容
Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子层结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于____________晶体,俗名为____________。
(2)R的氢化物分子的空间构型是____________;属于________分子(填“极性”或“非极性”)它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是____________。
(3)X的常见氢化物的空间构型是____________;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是____________。
(4)Q分别与Y、Z形成的共价化合物的化学式是________________和________________;Q与Y形成的分子的电子式是____________,属于____________分子(填“极性”或“非极性”)。
(1)分子 干冰
(2)正四面体 非极性 Si3N4
(3)三角锥形 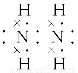
(4)CS2 CCl4 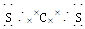 非极性
非极性
【解析】本题综合考查物质结构知识。根据题设条件可推知Q为C,R为Si,X为N,Y为S,Z为Cl。
(1)C的最高价氧化物为CO2,固态时是分子晶体,其俗名为干冰。
(2)Si的氢化物为SiH4,根据CH4的空间构型可知SiH4的空间构型为正四面体,SiH4分子中正负电荷重心重合,属于非极性分子。Si最外层有4个电子,N最外层有5个电子,它们形成化合物时,Si为+4价,N为-3价,其化学式为Si3N4。
(3)N的常见氢化物为NH3,其空间构型为三角锥形。根据N、H原子的成键原则,可得N2H4的结构简式为H2N—NH2,根据其结构简式可推写出其电子式。
(4)C与S可形成CS2,根据CO2的结构可写出CS2的电子式并知其为非极性分子。C与Cl形成CCl4分子。