题目内容
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X的质子数是Y的核外电子数的一半,Y与M可形成化合物M2Y,下列说法正确的是( )
| A、Z元素的最高价氧化物的水化物的化学式为HZO4 | B、离子半径:M的离子>Z的离子>Y的离子>X的离子 | C、X、M两元素形成的化合物只有M2X、M2X2两种 | D、还原性:X的氢化物>Y的氢化物>Z的氢化物 |
分析:X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X的核电荷数是Y的核外电子数的一半,应为同一主族元素,推测X为氧元素,则Y为硫元素,Z为氯元素;Y与M可形成化合物M2Y,则M为K元素,然后结合元素及其单质、化合物的性质来解答.
解答:解:X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X的核电荷数是Y的核外电子数的一半,应为同一主族元素,推测X为氧元素,则Y为硫元素,Z为氯元素;Y与M可形成化合物M2Y,则M为K元素,
A.Z为氯元素,其最高价氧化物的水化物为HClO4,故A正确;
B.电子层数越多,离子半径越大,具有相同电子排布的离子原子序数大的离子半径小,则离子的半径:Y的离子>Z的离子>M的离子>X的离子,故B错误;
C.O与K元素可形成K2O、K2O2、KO2等多种混合物,故C错误;
D.非金属性O>Cl>S,三种元素中S元素的非金属性最弱,因此其氢化物的还原性最强,则还原性为Y的氢化物>Z的氢化物>X的氢化物,故D错误.
故选A.
A.Z为氯元素,其最高价氧化物的水化物为HClO4,故A正确;
B.电子层数越多,离子半径越大,具有相同电子排布的离子原子序数大的离子半径小,则离子的半径:Y的离子>Z的离子>M的离子>X的离子,故B错误;
C.O与K元素可形成K2O、K2O2、KO2等多种混合物,故C错误;
D.非金属性O>Cl>S,三种元素中S元素的非金属性最弱,因此其氢化物的还原性最强,则还原性为Y的氢化物>Z的氢化物>X的氢化物,故D错误.
故选A.
点评:本题考查位置、结构、性质,熟悉元素周期律和元素周期表的相关知识,以及各知识点的综合应用即可解答,难度不大.

练习册系列答案
相关题目
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大。X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层电子数与其电子层数相等,Z—与M2+具有相同的核外电子层结构。下列推测正确的是( )
| A.原子半径Y>Z,离子半径Z—<M2+ |
| B.MX2与水发生反应时,MX2只做氧化剂 |
| C.X、Y形成的化合物既能与强酸反应又能与强碱反应 |
| D.MX2、MZ2两种化合物中,阳离子与阴离子个数比均为1:2 |

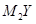 。下列说法正确的是(
)
。下列说法正确的是(
)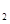 、M
、M