题目内容
15.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )| A. | 26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 标准状况下,B2H6和C2H4的混合气体22.4L,所含的电子数约为16NA | |
| D. | 标准状况下,1L庚烷所含有的分子数为NA/22.4 |
分析 A.C2H2和苯蒸气的混合气体最简式相同为CH,计算26gCH中含原子数;
B.1个甲基含有9个电子;
C.B2H6和C2H4中都含有16个电子;
D.气体摩尔体积只适用与气体.
解答 解:A.C2H2和苯蒸气的混合气体最简式相同为CH,计算26gCH中含原子数=$\frac{26g}{13g/mol}$×1×NA=2NA,故A正确;
B.1个甲基含有9个电子,1mol甲基(-CH3)所含电子数为9NA,故B正确;
C.B2H6和C2H4中都含有16个电子,标准状况下,B2H6和C2H4的混合气体22.4L的物质的量为1mol,含有电子数为16NA,故C正确;
D.标况下庚烷为液体,不能使用气体摩尔体积,故D错误;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下庚烷不是气体是解题关键,题目难度不大.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
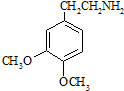
5. 丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
 丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )| A. | 萨罗的分子式为C13H10O3 | |
| B. | 丁子香酚和萨罗均能与氯化铁溶液发生显色反应 | |
| C. | 丁子香酚与浓溴水只发生取代反应 | |
| D. | 萨罗和丁子香酚均能发生氧化反应 |
6.下列互为同位素的一组是( )
| A. | 金刚石和石墨 | B. | mnX和wnX | ||
| C. | 质子数相同、中子数不同的微粒 | D. | 11H和21H |
10.下列各项中,表达正确的是( )
| A. | 乙醛的结构简式:CH3COH | B. | C2H2分子的结构式:CH≡CH | ||
| C. | CH4分子的比例模型: | D. | 异丁烷的键线式: |
20.下列原子的价电子构型中,第一电离能最小的是( )
| A. | 2s22p4 | B. | 3s23p4 | C. | 4s24p4 | D. | 5s25p4 |
7.下列有关元素周期表的说法中正确的是( )
| A. | 元素周期表有18个族 | |
| B. | 第IA族元素称为碱金属元素 | |
| C. | 原子最外层电子数相同的元素,一定属于同一族 | |
| D. | 第3列至第12列的元素全为金属元素 |

 .
.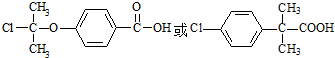 .
. (R、R′为烃基).根据已有知识并结合相关信息,写出以乙醇为原料制备
(R、R′为烃基).根据已有知识并结合相关信息,写出以乙醇为原料制备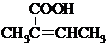 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: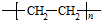

 .
. +CH3COOH$→_{△}^{浓H_{2}SO_{4}}$
+CH3COOH$→_{△}^{浓H_{2}SO_{4}}$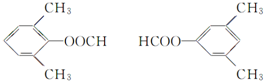 .
.