题目内容
【题目】高分子化合物V ( )是人造棉的主要成分之一,合成路线如下:
)是人造棉的主要成分之一,合成路线如下:

已知:I.
II.![]()
III.
(R、R1、R2、R3 表示烃基)
(1)A的名称是________________________。
(2)试剂a是__________________________。
(3) F与A以物质的量之比1∶1发生反应生成六元环状化合物H,H的结构简式是_______。
(4)I的结构简式是________________________。
(5)G的结构简式是_______________________________;E与J反应生成M的化学方程式是_______________________________________________。
(6)M与C反应生成V的化学方程式是____________________________。
(7)E的同分异构体N也可以和J反应生成M,N可能的结构简式是_______(写一种即可)。
【答案】 乙烯 NaOH水溶液 ![]() HOOC(CH2)4COOH CH3CH2OH
HOOC(CH2)4COOH CH3CH2OH 
 CH3OOCCOOCH(CH3)2 或CH3OOCCOOCH2CH2CH3
CH3OOCCOOCH(CH3)2 或CH3OOCCOOCH2CH2CH3
【解析】A为乙烯,乙烯与溴发生加成反应生成B为BrCH2CH2Br,B在氢氧化钠水溶液、加热条件下发生水解反应生成C为HOCH2CH2OH,C发生氧化反应得到D为HOOC-COOH,D与乙醇发生酯化反应生成E为CH3CH2OOCCOOCH2CH3。M与乙二醇反应得到V,结合V的结构简式可知M为 ,结合信息Ⅲ可知J为CH3CH2OOC(CH2)4COOCH2CH3,故I为HOOC(CH2)4COOH,G为CH3CH2OH,H为
,结合信息Ⅲ可知J为CH3CH2OOC(CH2)4COOCH2CH3,故I为HOOC(CH2)4COOH,G为CH3CH2OH,H为![]() 。
。
(1)A的名称是乙烯;(2)BrCH2CH2Br在氢氧化钠水溶液、加热条件下发生水解反应生成HOCH2CH2OH,试剂a是:氢氧化钠水溶液;(3)1,3-丁二烯与乙烯以物质的量之比1:1发生反应生成六元环状化合物H的结构简式是![]() ;(4)由上述分析可知,I的结构简式是HOOC(CH2)4COOH;(5)G为乙醇,结构简式为CH3CH2OH,E与J反应生成M的化学方程式是
;(4)由上述分析可知,I的结构简式是HOOC(CH2)4COOH;(5)G为乙醇,结构简式为CH3CH2OH,E与J反应生成M的化学方程式是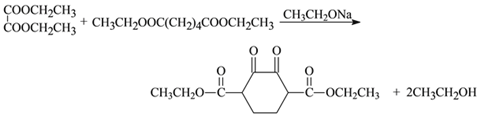 ;(6)M与C反应生成V的化学方程式是
;(6)M与C反应生成V的化学方程式是 ;(7)E的同分异构体N也可以和J反应生成M,N可能的结构简式是CH3OOCCOOCH(CH3)2 或CH3OOCCOOCH2CH2CH3。
;(7)E的同分异构体N也可以和J反应生成M,N可能的结构简式是CH3OOCCOOCH(CH3)2 或CH3OOCCOOCH2CH2CH3。

【题目】氨气是重要化工原料,在国民经济中占重要地位。工业合成氨的反应为: N2(g)+H2(g)=2NH3(g) △H<0
(1)右图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,t1、t3、t4 时刻分别改变某一外界条件,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是___________(填写下列序号)

A.t1→t1 B.t2→t3 C.t3→t4 D.t5→t6
t4时改变的条件是________________。
进行如下研究:在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
(2)该温度下,此反应的平衡常数K=____________。
(3)该温度下,若向同容积的另一容器中投入的N2、H2、NH3的浓度分别为3mo/L、3mol/L、3mo/L,则此时V正_____V逆 (填">"“<”或“=”)。
(4)由上表中的实验数据计算得到“浓度一时间”的关系可用右图中的曲线表示,表示c(N2)-t的曲线是______。在此温度下,若起始充入4molN2和12 molH2,则反应刚达到平衡时,表示c(H2)-t的曲线上相应的点为_________。

【题目】某化学小组采用类似制乙酸乙酯的装置,用环己醇制备环己烯:
已知: 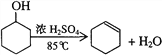
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
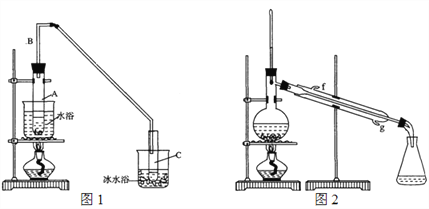
(1)制备粗品:采用如图1所示装置,用环己醇制备环己烯。
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_____________,导管B的作用是_______________。
②试管C置于冰水浴中的目的是________________________。
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在______层(填“上”或“下”),分液后用________洗涤(填字母)。
A. KMnO4溶液 B. 稀H2SO4 C. Na2CO3溶液
②再将环己烯按图2装置蒸馏,冷却水从____口(填字母)进入。蒸馏时加入生石灰,目的是______________________________________。
③收集产品时,控制的温度应在______左右,实验制得的环己烯精品质量低于理论产量,可能的原因是______(填字母)。
a. 蒸馏时从70℃开始收集产品
b. 环己醇实际用量多了
c. 制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是________(填字母)。
a. 用酸性高锰酸钾溶液
b. 用金属钠
c. 测定沸点



