题目内容
8.根据所学化学知识解答以下小题:(1)写出硫酸氢钠在水溶液中的电离方程式NaHSO4=Na++H++SO42-
(2)卫星发射时可用肼(N2H4)做燃料,1mol N2H4(L)在氧气(g)中燃烧,生成氮气(g)和水(L),放出622KJ热量.请书写该反应的热化学方程式N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622kJ/mol
(3)写出H2S在水溶液中的电离方程式H2S
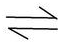 HS-+H+
HS-+H+(4)写出H2SO4溶液与Na2S2O3溶液反应的离子方程式S2O32-+2H+=S+SO2+H2O
(5)下列物质中,能导电的是①③?⑦⑧,属于电解质的是?④⑤⑧
①Cu ②H2SO4 ③NaCl溶液 ④NaOH ⑤BaSO4 ⑥蔗糖 ⑦石墨 ⑧熔融KCl.
分析 (1)硫酸氢钠为强电解质,完全电离;
(2)写出反应方程式,注明物质的聚集状态,依据反应物用量与反应放出热量写出热化学方程式;
(3)硫化氢为弱电解质,分步电离,以第一步为主;
(4)二者反应生成硫单质和二氧化硫、水和硫酸钠;
(5)物质导电的条件是含有自由电子或者自由离子;在水溶液中或者熔融状态下能够导电的化合物是电解质;在水溶液中和熔融状态下都不导电,属于非电解质.
解答 解:(1)硫酸氢钠为强电解质,完全电离,电离方程式:NaHSO4=Na++H++SO42-,
故答案为:NaHSO4=Na++H++SO42-;
(2)卫星发射时可用肼(N2H4)做燃料,1mol N2H4(L)在氧气(g)中燃烧,生成氮气(g)和水(L),放出622KJ热量,反应的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622 kJ/mol;
故答案为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622 kJ/mol;
(3)硫化氢为弱电解质,分步电离,以第一步为主,电离方程式:H2S  HS-+H+,
HS-+H+,
故答案为:H2S  HS-+H+;
HS-+H+;
(4)H2SO4溶液与Na2S2O3溶液反应,离子方程式:S2O32-+2H+=S+SO2+H2O;
故答案为:S2O32-+2H+=S+SO2+H2O;
(5)①Cu是单质,含有自由电子,能够导电不是电解质;
②H2SO4 不含自由电子或者自由离子,不导电;在水溶液中能导电,属于电解质;
③NaCl溶液含有自由离子,能够导电;是混合物,不是电解质;
④NaOH 不含自由电子或者自由离子,不导电;在水溶液中或者熔融状态下能够导电,属于电解质;
⑤BaSO4 不含自由电子或者自由离子,不导电;熔融状态下能够导电,属于电解质;
⑥蔗糖不含自由电子或者自由离子,不导电;在水溶液中和熔融状态下都不导电,属于非电解质;
⑦石墨含有自由电子,能够导电;是单质,不是电解质;
⑧熔融KCl含有自由离子,能够导电;在水溶液中或者熔融状态下能够导电,属于电解质;
能导电的是①?③⑦⑧;属于电解质的是:④⑤⑧;
故答案为:①?③⑦⑧;?④⑤⑧.
点评 本题考查了电解质电离方程式、离子方程式书写,电解质判断,题目难度不大,掌握基础是关键.

 名校课堂系列答案
名校课堂系列答案| A. | c(Z)=0.3mol/L | B. | c(X2)=0.3mol/L | C. | c(Y2)=0.2mol/L | D. | c(Z)=0.4mol/L |
| A. | 酶是具有催化作用的蛋白质 | |
| B. | 酶的催化作用具有选择性和专一性 | |
| C. | 强酸性或强碱性条件下能降低酶的活性 | |
| D. | 使用热水和加酶洗衣粉能提去污能力 |
| A. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| A. | 浓盐酸 | B. | 浓氢氧化钠溶液 | C. | 硫酸 | D. | 硝酸 |
| A. | 1 mol CH3COOK的质量为98 g•mol-1 | |
| B. | CH3COOK的摩尔质量等于它的相对分子质量 | |
| C. | 一个CH3COOK微粒的质量约为98 g/NA | |
| D. | 含有6.02×1023个碳原子的CH3COOK的物质的量为1 mol |
| A. | Cu2++2OH-═Cu(OH)2↓ CuSO4+Ba(OH)2═Cu(OH)2↓+BaSO4↓ | |
| B. | CO32-+2H+═CO2↑+H2O NaHCO3+HCl═NaCl+CO2↑+H2O | |
| C. | H++OH-═H2O NaOH+HNO3═NaNO3+H2O | |
| D. | SO42-+Ba2+═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O |
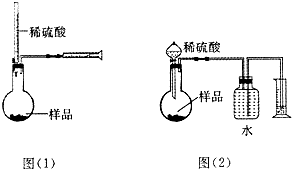 为测定NaOH、Na2C03混合物中Na2C03的质量分数,甲同学拟采用图(1)所示装置来测定.乙同学拟采用图(2)所示装置来测定.请回答下列问题:
为测定NaOH、Na2C03混合物中Na2C03的质量分数,甲同学拟采用图(1)所示装置来测定.乙同学拟采用图(2)所示装置来测定.请回答下列问题: