题目内容
接触法制硫酸,最后的产品是质量分数为98%的硫酸或20%的发烟硫酸(H2SO4和SO3的混合物,其中含20%的SO3)。(1)若98%硫酸可表示为SO3·aH2O,20%发烟硫酸可表示为H2O·bSO3,则a、b的值(可用分数表示)分别是:a=_____________、b=______________。
(2)若用m(H2O)=k·n(SO3)分别表示SO3转化成98%的硫酸和20%发烟硫酸时需水的质量与SO3物质的量的关系式,则有:m1(H2O)=______________n1(SO3),m2(H2O)=__________n2(SO3)。
解析:(1)根据题意,假设产品质量都为100 g,则纯H2SO4 98 g,H2O 2 g。
故n(H2SO4)∶n(H2O)=![]() ∶
∶![]() =1∶
=1∶![]() ,
,
所以有H2SO4·![]() H2O
H2O![]() ?SO3·H2O·
?SO3·H2O·![]() H2O
H2O![]() SO3·
SO3·![]() H2O。即a=
H2O。即a=![]() 。
。
20%的发烟硫酸需纯H2SO4 80 g,SO3 20 g。
故n(H2SO4)∶n(SO3)=![]() ∶
∶![]() =
=![]() ∶
∶![]() 。
。
所以有![]() H2SO4·
H2SO4·![]() SO3
SO3![]()
![]() SO3·
SO3·![]() H2O·
H2O·![]() SO3
SO3![]() (
(![]() +
+![]() )SO3·
)SO3·![]() H2O
H2O![]()
![]() SO3·
SO3·![]() H2O
H2O![]()
![]() SO3·H2O。即b=
SO3·H2O。即b=![]() 。
。
(2)根据题给信息,仍设产品质量为100 g,由m(H2O)=k·n(SO3)可分别求出98%的硫酸和20%的发烟硫酸的k值。
98%的硫酸:m(H2O)=2+18=20 g,n1(SO3)=1 mol,
则k1=20 g/1 mol=20 g·mol-1,
所以m1(H2O)=20 g·mol-1·n1(SO3)
20%的发烟硫酸:由(1)计算结果知,m(H2O)=![]() ,n2(SO3)=
,n2(SO3)=![]() mol,
mol,
则k2=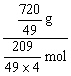 =13.8 g·mol-1,
=13.8 g·mol-1,
所以m2(H2O)=13.8 g·mol-1·n2(SO3).
答案:(1)![]()
![]()
(2)20 g·mol-1 13.8 g·mol-1

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目