题目内容
对于热化学方程式:SO3(g)?SO2(g)+1/2O2(g);△H=+98.3kJ?mol-1的描述有如下四个图象,其中正确的是(y表示SO2的含量)( )
A.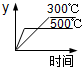 | B.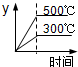 | C.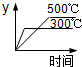 | D.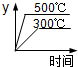 |
该反应正反应是吸热反应,温度越高,反应速率越快,到达平衡的时间越短,升高温度平衡向正反应移动,平衡时SO2的含量增大,
A、正反应是吸热反应,升高温度平衡向正反应移动,平衡时SO2的含量增大,图象中温度越高,到达平衡时SO2的含量越低,与实际不符合,故A错误;
B、温度越高,反应速率越快,到达平衡的时间越短,图象中300℃与500℃到达平衡的时间相同,故B错误;
C、温度越高,反应速率越快,到达平衡的时间越短,图象中300℃比500℃早达平衡,故C错误;
D、图象中500℃到达平衡的时间短,平衡时平衡时SO2的含量高,与实际相符合,故D正确;
故选D.
A、正反应是吸热反应,升高温度平衡向正反应移动,平衡时SO2的含量增大,图象中温度越高,到达平衡时SO2的含量越低,与实际不符合,故A错误;
B、温度越高,反应速率越快,到达平衡的时间越短,图象中300℃与500℃到达平衡的时间相同,故B错误;
C、温度越高,反应速率越快,到达平衡的时间越短,图象中300℃比500℃早达平衡,故C错误;
D、图象中500℃到达平衡的时间短,平衡时平衡时SO2的含量高,与实际相符合,故D正确;
故选D.

练习册系列答案
相关题目