题目内容
【题目】NH3及其盐都是重要的化工原料. 
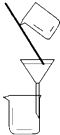
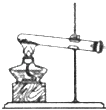
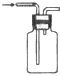
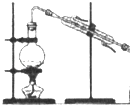
(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为;该反应发生、气体收集和尾气处理装置如图1依次为;
(2)按如图2装置进行NH3性质实验.先打开旋塞1,B瓶中的现象是 , 稳定后,关闭旋塞1.再打开旋塞2,B瓶中的现象是;
(3)写出NH4Cl溶液水解的离子方程式; 设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响.
限选试剂与仪器:固体NH4Cl、蒸馏水、250mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究对溶液中NH4Cl水解程度的影响;
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积).
物理量 | V(溶液)/mL | NH4Cl质量/g | 温度/℃ | … | |
1 | 250 | X | … | ||
2 | 250 | … |
③按实验序号1所拟数据进行实验,若读取的待测物理量的数值为X,则NH4Cl水解反应的平衡转化率为(只列出算式,忽略水自身电离的影响).
【答案】
(1)2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;BDE
CaCl2+2NH3↑+2H2O;BDE
(2)产生白色的烟;烧杯中的石蕊溶液会倒吸入B瓶,且溶液变为红色
(3)NH4++H2O?NH3?H2O+H+;温度;pH;m;T1;m;T2;Y;![]()
【解析】解:(1)NH4Cl和Ca(OH)2在加热条件下生成氨气、氯化钙和水,化学方程式:2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;反应物为固体与固体和反应条件为加热,所以选择B发生装置,氨气易溶于水,密度小于空气密度应选择向下排空气法收集,所以选择D收集装置,氨气极易溶于水,可以用水吸收,注意防止倒吸的发生,可选择E做尾气处理装置; 故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;反应物为固体与固体和反应条件为加热,所以选择B发生装置,氨气易溶于水,密度小于空气密度应选择向下排空气法收集,所以选择D收集装置,氨气极易溶于水,可以用水吸收,注意防止倒吸的发生,可选择E做尾气处理装置; 故答案为:2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;BDE;(2)氯化氢与氨气反应生成白色固体氯化铵,所以看到现象为:产生白色的烟;
CaCl2+2NH3↑+2H2O;BDE;(2)氯化氢与氨气反应生成白色固体氯化铵,所以看到现象为:产生白色的烟;
氨气溶于水生成一水合氨,一水合氨电离生成氢氧根离子和铵根离子,溶液显碱性,所以看到现象为:烧杯中的石蕊溶液会倒吸入B瓶,且溶液变为红色;
故答案为:产生白色的烟;烧杯中的石蕊溶液会倒吸入B瓶,且溶液变为红色;(3)氨根离子为弱碱阳离子,水解生成一水合氨和氢离子,水解的离子方程式:NH4++H2ONH3H2O+H+;
故答案为:NH4++H2ONH3H2O+H+;①盐类水解,水解离子浓度越大,水解程度越小,盐类水解为吸热反应,温度越高,水解程度越大,根据题干提供的限选试剂与仪器中的温度计、恒温水浴槽(可调控温度),可选择温度不同对盐类水解的影响,
故答案为:温度;②根据①可知,该实验为探究温度对氯化铵水解的影响,氯化铵为强酸弱碱盐,水解溶液呈酸性,所以可根据不同温度下,水解的溶液的pH进行判断,所配制溶液的体积都为100mL,m(NH4Cl)相同都为m g,温度不同,分别为T1℃、T2℃,分别测水解后pH;
故答案为:
物理量 | V(溶液)/mL | NH4Cl质量(g) | 温度(℃) | pH | … |
1 | m | T1 | … | ||
2 | m | T2 | Y | … |
③读取的待测物理量的数值为X,X为pH值,pH=﹣lgc(H+),c(H+)=10﹣Xmol/L,NH4++H2ONH3H2O+H+ , 水解的氯化铵的物质的量为n(NH4Cl)=c(H+)×V=10﹣X×0.25mol,则NH4Cl水解反应的平衡转化率为: ![]() ×100%=
×100%= ![]() ×100%;
×100%;
故答案为: ![]() .
.
(1)NH4Cl和Ca(OH)2在加热条件下生成氨气、氯化钙和水;依据反应物状态和条件选择发生装置,依据氨气易溶于水,密度小于空气密度选择收集装置,依据氨气极易溶于水选择尾气处理装置;(2)氯化氢与氨气反应生成固体氯化铵;氨气溶于水生成一水合氨,一水合氨电离生成氢氧根离子和铵根离子,溶液显碱性;(3)氨根离子为弱碱阳离子,水解生成一水合氨和氢离子;①根据影响NH4Cl水解的因素以及题干提供的限选试剂与仪器分析;②氯化铵为强酸弱碱盐,水解溶液呈酸性,所配制溶液的体积,根据温度不同,盐类水解后PH不同,进行设计表格数据;③读取的待测物理量的数值为X,X为PH值,PH=﹣lgc(H+)可求算出氢离子浓度,根据NH4++H2ONH3H2O+H+ , 求解NH4Cl水解反应的平衡转化率.