题目内容
下列说法正确的是( )
| A.浓硫酸溶于水的过程属于放热反应 |
| B.既有化学键断裂又有化学键生成的过程一定属于化学反应 |
| C.物质导电的过程一定是物理变化 |
| D.同分异构体之间的相互转化一定是化学变化 |
D
解析试题分析:A选项放热反应是相对于化学反应来说的,而浓硫酸溶于水,存在物理变化和化学变化,因此A选项是错误的,B选项化学变化的本质是旧键的断裂和新建的形成过程。例如氯化钠晶体受热熔化只有旧键断裂,等氯化钠又恢复为原来的温度时,又形成了原来的化学键,这个过程属于物理变化,因此B选项是错误的。
考点:考查化学键的相关知识点

练习册系列答案
相关题目
下列反应的离子方程式正确的是
| A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H+十SO42-="=" BaSO4↓+H2O |
| B.稀碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3- + OH- ="=" CO32- + H2O |
| C.氯化铝溶液中滴加过量氨水:Al3+ + 3NH3·H2O="=" Al(OH)3↓+ 3NH4+ |
| D.常温下,将铜片加入稀硝酸中:Cu + 2H+ ="=" Cu2+ + 2H2↑ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.无色溶液中:K+、H+、Fe2+、NO3- |
| B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- |
| C.含0.1mol·L-1 HCO3-的溶液中:Al3+、Ca2+、NO3-、SO42- |
| D.含0.1 mol·L-1 SCN-的溶液中:Fe3+、NH4+、NO3-、Cu2+ |
下列反应的离子方程式正确的是
| A.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| B.铜片加入浓硝酸中:3Cu+4H++NO3-=3Cu2++NO↑+2H2O |
C.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| D.AlCl3溶液中加入足量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
常温下,下列各组微粒在指定的溶液中一定能大量共存的是
| A.c(OH—)=10—13mol·L—1的溶液中:Na+、NH4+、Cl—、NO3— |
| B.1.0 mol·L—1KI溶液中:Mg2+、Fe2+、SO42—、C1O— |
| C.c(Fe3+)="0.1" mol·L-1的溶液中:Na+、NH4+、HCO3-、SCN— |
| D.饱和氨水中:NH4+、Ag+、SO42-、NO3— |
下列化学反应的离子方程式正确的是
| A.FeCl3与氨水反应:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ |
B.铜与稀硝酸反应:Cu+8H++2NO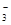 =Cu2++2NO↑+4H2O =Cu2++2NO↑+4H2O |
| C.NO2与水反应:3NO2+H2O=NO3-+NO+2H+ |
| D.醋酸与CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
下列离子方程式正确的是
| A.MgSO4溶液中加入Ba(OH)2溶液:Ba2++SO4 2-=BaSO4↓ |
| B.FeCl3溶液中加入Cu粉:2Fe3++3Cu=2Fe+3Cu2+ |
| C.酸性碘化钾溶液中滴加双氧水:2I-+2H+ +H2O2=I2+2H2O |
| D.氯化铝溶液中滴加氨水:Al3++4OH-=AlO2-+2H2O |
下列表示对应化学反应的离子方程式正确的是
A.MnO2固体与浓盐酸反应制取Cl2:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| B.AlCl3溶液中滴加浓氨水至过量:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| C.氯化亚铁溶液中加入硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
D.NH4HCO3溶于过量的NaOH溶液中:HCO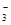 +OH-===CO +OH-===CO +H2O +H2O |