题目内容
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | FeCl3溶液能腐蚀Cu | Fe的金属性强于Cu |
| B | Na2O2使酚酞溶液变红 | Na2O2使品红溶液褪色 |
| C | Cl2可部分与水反应 | 用排饱和食盐水法收集Cl2 |
| D | 浓H2SO4可干燥NO和SO2 | NO和SO2还原性都弱 |
C
解析试题分析:A、FeCl3溶液能腐蚀Cu,发生的反应为:2Fe3++Cu=2Fe2++Cu2+,与Fe的金属性强于Cu无关;B、Na2O2使酚酞溶液先变红后褪色,错误;C、Cl2可部分与水反应,饱和食盐水中Cl?浓度大,降低了Cl2的溶解度,所以用排饱和食盐水法收集Cl2,正确;D、浓硫酸可干燥SO2,是因为浓硫酸中的S元素为+6价,SO2中的S元素为+4价,二者不能发生氧化还原反应,错误。
考点:本题考查物质的性质。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
实验室中以下物质的贮存方法不正确的是
| A.浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
| B.保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 |
| C.少量金属钠保存在煤油中 |
| D.试剂瓶中的液溴可用水封存,防止溴挥发 |
化学与社会、生产、生活紧切相关,下列说法正确的是
①石英只可用于生产光导纤维,且常温下不与任何酸反应;
②次氯酸钠溶液可用于环境的消毒杀菌;
③黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成;
④用铜片在加热的条件下就可鉴别浓硫酸和稀硫酸;
⑤70mL的H2S和90mL的O2混合点燃后恢复到原状况可产生70mL的SO2;
⑥将过量CO2气体通入水玻璃中可生成硅酸和纯碱
| A.①②④⑤ | B.①②③④ | C.②④⑥ | D.②③④ |
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是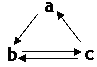
| | a | b | c |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | SO3 | H2SO4 | S |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 氯气具有强还原性 | 可用于自来水的消毒杀菌 |
| B | SiO2导电能力强 | 可用于制造通讯光缆 |
| C | 常温下铝在浓硫酸中钝化 | 常温下可用铝制容器盛放浓硫酸 |
| D | Na2S还原性强 | 用于除去废水中的Cu2+和Hg2+ |
下列说法不正确的是
| A.二氧化硫不能用于食品增白 |
| B.Cl2溶于氢氧化钠溶液可以制取84消毒液 |
| C.SiO2不溶于强酸,因而它可以保存在玻璃试剂中 |
| D.NO遇空气变成红棕色 |
现有H2SO4、Ba(OH)2、Na2CO3和氯水4种溶液,有如图所示的相互关系,图中每条线段两端的物质可以发生化学反应。下列推断合理的是
| A.M一定是Ba(OH)2 |
| B.Y可能是氯水 |
| C.X一定是Na2CO3溶液 |
| D.Z可能是H2SO4 |
根据下列实验现象,所得结论正确的是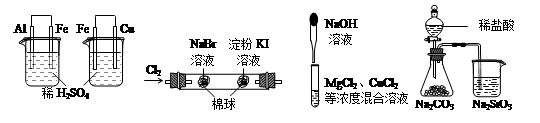
A B C D
| 实验 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 先生成蓝色沉淀,后产生白色沉淀 | 溶度积常数:Mg(OH)2<Cu(OH)2 Cu(OH)2Mg(OH)2<Cu(OH)2MgMg(OH)2<Cu(OH)2Mg(OH)2<Cu(OH)2 |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
下列各项反应对应的图像正确的是( )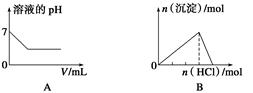
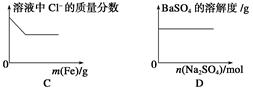
| A.25 ℃时,向亚硫酸溶液中通入氯气 |
| B.向NaAlO2溶液中通入HCl气体 |
| C.向少量氯化铁溶液中加入铁粉 |
| D.向BaSO4饱和溶液中加入硫酸钠 |