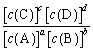ĢāÄæÄŚČŻ
¶ŌÓŚ·“Ó¦aA+bBƒcC+dD·“Ó¦“ļĘ½ŗāŹ±£¬Ė²Ź±ĖŁĀŹvÕż=k1[c(A)]a[c(B)]b£¬vÄę=
k2[c(C)]c[c(D)]d£¬ĘäÖŠ ![]() ”¢
”¢![]() ĪŖĖŁĀŹ³£Źż”£“ļĘ½ŗāŹ± k=
ĪŖĖŁĀŹ³£Źż”£“ļĘ½ŗāŹ± k=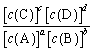 £¬ĒŅ
£¬ĒŅ![]() ”¢
”¢![]() ”¢kÖ»ÓėĪĀ¶ČÓŠ¹Ų”£ĻÖ½«4mol
SO2ŗĶ2mol O2³äČėČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬500”ę½ųŠŠ·“Ó¦²¢±£³ÖĪĀ¶Č²»±ä£¬·“Ó¦“ļĘ½ŗāŹ±£¬SO2×Ŗ»ÆĀŹĪŖ50%”£Ōņ£ŗ
”¢kÖ»ÓėĪĀ¶ČÓŠ¹Ų”£ĻÖ½«4mol
SO2ŗĶ2mol O2³äČėČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬500”ę½ųŠŠ·“Ó¦²¢±£³ÖĪĀ¶Č²»±ä£¬·“Ó¦“ļĘ½ŗāŹ±£¬SO2×Ŗ»ÆĀŹĪŖ50%”£Ōņ£ŗ
£Ø1£©ĘšŹ¼Ź±Õż·“Ó¦ĖŁĀŹŹĒĘ½ŗāŹ±µÄ________±¶”£
£Ø2£©ŌŚ500”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżkŹĒ________”£
£Ø3£©ŌŚĪĀ¶Č²»±äŹ±ŌŁĻņĘ½ŗāĢåĻµÖŠ¼ÓČė2mol SO2”¢2mol O2ŗĶ4mol SO3£¬Ę½ŗā½«Ļņ________ŅĘ¶Æ”£
“š°ø£ŗ
½āĪö£ŗ
ĢįŹ¾£ŗ
½āĪö£ŗ
£Ø1£©8 £Ø2£©2L”Įmol-1 £Ø3£©ÓŅ£Ø»ņÕż·“Ó¦·½Ļņ£©
|
ĢįŹ¾£ŗ
ĢįŹ¾£ŗ2SO2 + O2ƒ2SO3 4mol 2mol 0 -2mol -1mol +2mol vÕż£ØĘšŹ¼£©”ĆvÕż£ØĘ½£©= 500”ꏱ£¬k= Ę½ŗāĢåĻµÖŠ¼ÓČėĪļÖŹŗó£¬c(SO2)=2mol”ĮL-1£¬c(O2)=1.5mol L-1£¬c(SO3)=3mol”ĮL-1£¬“ĖŹ±ÅØ¶Č¹ŲĻµĪŖ£ŗ k¢=
|

Į·Ļ°²įĻµĮŠ“š°ø
Ļą¹ŲĢāÄæ