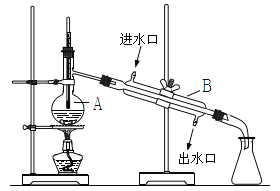
题目内容
【题目】实验室制取Cl2及性质的验证实验组合装置如下:
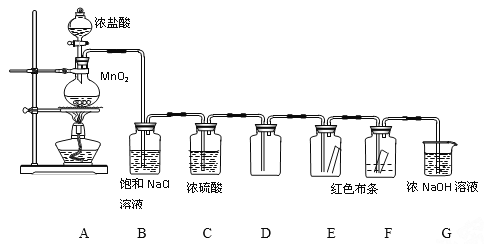
回答下列问题:
(1)A中的化学方程式为____________________________________。
(2)B的作用是除去HCl气体,C的作用是________________________________。
(3)E、F中观察到的现象分别是________________,你得到的结论是________。
(4)G的作用是____________,离子方程式为________________________。
【答案】 4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O 除去氯气中的水蒸气,得到干燥的氯气,防止对E中实验的干扰 E中红色布条不褪色,F中红色布条褪色 说明干燥的Cl2没有漂白性,Cl2与水反应的某种产物具有漂白性 防止尾气中的氯气污染空气 Cl2+2OH-=Cl-+ClO-+H2O
MnCl2+Cl2↑+2H2O 除去氯气中的水蒸气,得到干燥的氯气,防止对E中实验的干扰 E中红色布条不褪色,F中红色布条褪色 说明干燥的Cl2没有漂白性,Cl2与水反应的某种产物具有漂白性 防止尾气中的氯气污染空气 Cl2+2OH-=Cl-+ClO-+H2O
【解析】(1)A中浓盐酸被二氧化锰氧化生成氯气,反应的化学方程式为4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O,故答案为:4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O,故答案为:4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)生成的氯气中往往含有氯化氢和水蒸气,B的饱和食盐水了可以除去HCl气体,C中浓硫酸可以干燥氯气,除去水蒸气,防止对E中实验的干扰,故答案为:除去氯气中的水蒸气,得到干燥的氯气,防止对E中实验的干扰;
(3)干燥的氯气没有漂白性,次氯酸具有漂白性,因此E、F中观察到的现象分别是E中红色布条不褪色,F中红色布条褪色,故答案为:E中红色布条不褪色,F中红色布条褪色;干燥的Cl2没有漂白性,Cl2与水反应的某种产物具有漂白性;
(4)氯气有毒,会污染空气,G中的氢氧化钠可以吸收多余的氯气,防止污染空气,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:防止尾气中的氯气污染空气;Cl2+2OH-=Cl-+ClO-+H2O。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是

选项 | W | X |
A | 盐 酸 | Na2CO3溶液 |
B | Cl2 | Fe |
C | CO2 | Ca(OH)2溶液 |
D | NaOH溶液 | AlCl3溶液 |
A. A B. B C. C D. D