题目内容
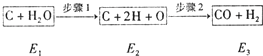 如图是炭和水蒸汽发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应.试问:
如图是炭和水蒸汽发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应.试问:(1)步骤1、2分别是吸热过程还是放热过程?步骤1:
吸热过程
吸热过程
;步骤2:放热过程
放热过程
;(2)比较E1、E2、E3的大小:
E2>E1>E3
E2>E1>E3
.(用“>”、“<”或“=”连接)分析:根据放热过程生成物的总能量小于反应物总能量,吸热过程生成物的总能量高于反应物总能量,结合炭和水蒸汽发生反应生成CO、H2为放热反应判断;
根据反应热等于生成物的总能量-反应物的总能量,然后根据物质的物质的量与反应热的关系计算;吸热反应中化学键断裂形成原子需要吸收能量大于原子之间形成化学键放出能量.
根据反应热等于生成物的总能量-反应物的总能量,然后根据物质的物质的量与反应热的关系计算;吸热反应中化学键断裂形成原子需要吸收能量大于原子之间形成化学键放出能量.
解答:解:(1)步骤l中化学键断裂形成原子,应是吸热过程,步骤2是原子之间形成化学键生成新物质,放出热量;
故答案为:吸热过程,放热过程;
(2)步骤1为吸热过程,故E2>E1,步骤2是放热过程,故E2>E3,由于炭和水蒸汽发生反应生成CO、H2为吸热反应,故E1>E3,故E2>E1>E3;
故答案为:E2>E1>E3 ;
故答案为:吸热过程,放热过程;
(2)步骤1为吸热过程,故E2>E1,步骤2是放热过程,故E2>E3,由于炭和水蒸汽发生反应生成CO、H2为吸热反应,故E1>E3,故E2>E1>E3;
故答案为:E2>E1>E3 ;
点评:本题考查了化学反应的实质,断裂化学键吸收能量,形成化学键放出热量,题目难度中等.

练习册系列答案
相关题目