题目内容
设NA为阿伏加德罗常数的值。下列叙述中,正确的是
| A.12.0gNaHSO4晶体中阳离子和阴离子的总数为0.3 NA |
| B.14g分子式CnH2n的链烃中含有的碳碳双键的数目一定为NA/n |
| C.标准状况下,1L液态水中含有的H+数目为10-7NA |
| D.足量Zn与一定量的浓硫酸反应,产生22.4L气体时,转移的电子数为2 NA |
B
解析试题分析:A、12.0gNaHSO4的物质的量是0.1mol,晶体中阳离子和阴离子的总数为0.2NA,A不正确;B、分子式CnH2n的链烃是烯烃,分子中含有1个碳碳双键,所以14g分子式CnH2n的链烃中含有的碳碳双键的数目一定为NA/n,B正确;C、标准状况下水中氢离子浓度小于10-7mol/L,所以标准状况下,1L液态水中含有的H+数目小于10-7NA,C不正确;D、气体的状态不能确定,因此不能计算转移电子的物质的量,D不正确,答案选B。
考点:考查阿伏伽德罗常数的有关计算

练习册系列答案
相关题目
下列有关概念间关系的说法正确的是
| A.碱性氧化物一定是金属氧化物 |
| B.氧化剂在化学反应中一定被氧化 |
| C.酸性氧化物一定是非金属氧化物 |
| D.摩尔质量相同的物质其摩尔体积一定相同 |
下列物质中,既有离子键,又有共价键的是
| A.CaCl2 | B.Na2O | C.H2O | D.NH4Cl |
下列化学用语或模型正确的是
A.氯化氢的电子式: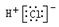 |
| B.8个中子的碳原子:12C |
C.硫离子结构示意图: |
D.CH4分子的比例模型: |
有关化学用语正确的是 ( )
| A.溴乙烷的分子式C2H5Br |
| B.乙醇的结构简式C2H6O |
C.四氯化碳的电子式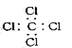 |
| D.乙烯的结构简式CH2CH2 |
下列有关化学用语或名称,表达错误的是
A.COCl2分子的结构式: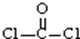 |
B.苯分子的比例模型: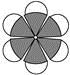 |
| C.铁在潮湿的空气中腐蚀,负极的电极反应式:Fe-2e-===Fe2+ |
D.溴化铵的电子式: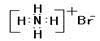 |
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度、密度相等时,下列说法正确的是
| A.两种气体的压强相等 |
| B.O2比O3质量小 |
| C.两种气体的分子数目相等 |
| D.两种气体的氧原子数目相等 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 L 0.1 mol·L-1的氨水中含有NH3·H2O分子数为0.1NA |
| B.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA |
| C.标准状况下,2.24 L的二氯甲烷中含有的碳氯共价键的数目为0.2NA |
| D.一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA |