题目内容
下列物质转化在给定条件下能实现的是
①FeS2 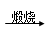 SO3
SO3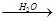 H2SO4
H2SO4 CO2
CO2
② Al2O3 NaAlO2(aq)
NaAlO2(aq) Al(OH)3
Al(OH)3
③NaCl(aq) Na
Na  NaOH(aq)
NaOH(aq)
④Fe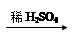 FeSO4(aq)
FeSO4(aq) Fe(OH)2
Fe(OH)2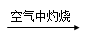 Fe2O3
Fe2O3
⑤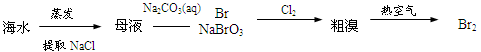
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
C
解析试题分析:①中煅烧FeS2得到到SO2不是SO3,错误;③NaCl(aq)是氯化钠的水溶液,若电解其水溶液得到是NaOH,电解熔融NaCl可制得金属钠,错误;
考点:考查常见物质的工业生产基本原理和基本元素化合物转化关系。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述不正确的是( )
| A.金属X能与NaOH溶液反应放出H2,但金属Y不能,则Y的金属性一定比X弱 |
| B.在合成氨反应达到平衡时,只增加N2的物质的量,达新平衡后N2的百分含量增大 |
| C.在铁件上镀铜时,铁和电源负极相连,铜和正极相连,电解质溶液是CuSO4溶液 |
| D.Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
向红色溶液X中通入气体Y,溶液逐渐褪色,下列对X、Y的推断正确的是
| A.若X为品红溶液,则Y可能为CO2或SO2 |
| B.若X为含酚酞的NaOH溶液,则Y可能是O3 |
| C.若X为含KSCN的FeCl3溶液,则Y一定为HI |
| D.若X为含少量KMnO4的H2SO4溶液,则Y一定为SO2 |
对下列实验的现象描述正确的是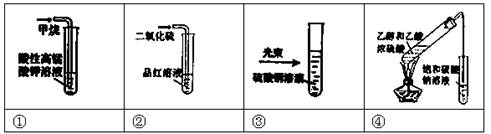
| A.实验①溶液褪色 | B.实验③溶液中看到一条光亮的通路 |
| C.实验②溶液褪色 | D.实验④饱和碳酸钠溶液下方出现油状液体 |
类比推断法是研究物质性质的常用方法之一,可预测许多物质的性质。但类比推断法是相对的,不能违背客观实际。下列说法正确的是
| A.由溶解性CaCO3<Ca(HCO3)2,则溶解性Na2CO3<NaHCO3 |
| B.向Ca(ClO)2溶液中通入少量CO2可得到CaCO3,则向Ca(ClO)2溶液中通入少量SO2可得到CaSO3 |
| C.由O2与Li加热生成Li2O,则O2与Na加热生成Na2O |
| D.有Fe与S加热生成FeS,则Cu与S加热生成Cu2S |
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验:
下列有关说法正确的是
| A.步骤I中减少的3g固体一定是混合物 |
| B.步骤II中质量减少的物质一定是Cu |
C.根据上述步骤II可以得出 |
| D.根据步骤I、II可以判断混合物X的成分为Al2O3、Fe2O2、Cu、SiO2 |
甲、乙、丙有如图转化关系:甲 乙
乙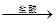 丙
丙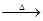 甲,甲不可能是
甲,甲不可能是
| A.A12O3 | B.SiO2 | C.NH4C1 | D.CO2 |
下列说法不正确的是
| A.将Na2O2投入NH4Cl溶液中只可能生成一种气体 |
| B.铁分别与稀盐酸和硫反应,产物中铁元素的化合价相同 |
| C.向饱和ZnS溶液中加入Na2S有沉淀析出,但Ksp(ZnS)不变 |
| D.在滴有酚酞的Na2CO3溶液中,加入适量BaCl2溶液后溶液褪色 |
重氧(18O)是氧元素的一种放射性同位素,下列说法正确的是
| A.Na2O2与H218O反应时生成18O2气体 |
B.向2SO2(g)+O2(g) 2SO3(g)的平衡体系中加入18O2,结果18O只出现在SO3中 2SO3(g)的平衡体系中加入18O2,结果18O只出现在SO3中 |
| C.CH3COOH和CH3CH218OH发生酯化反应时,产物水的分子式为H218O |
| D.用惰性电极电解含有H218O的水时,阳极会产生三种相对分子质量不同的氧分子 |