题目内容
20.00 mL一定物质的量浓度的盐酸X,用一定浓度的NaOH溶液Y滴定,如图所示。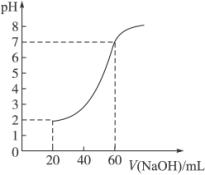
(1)试求X和Y的物质的量浓度之比。
(2)求盐酸的物质的量浓度。
(1)c(X)∶c(Y)=3∶1 (2)c(HCl)=0.030 mol·L-1 解析:完全中和时V(HCl)=20 mL,V(NaOH)=60 mL,故c(HCl)∶c(NaOH)=60∶20=3∶1 V(NaOH)=20 mL时,则中和HCl的1/3,此时c(H+)=0.01 mol·L-1 (pH=1),溶液总体积为20 mL+20 mL=40 mL n(H+)=0.01 mol·L-1×0.04 L=4×10-4 mol HCl的总n(H+)=4×10-4 mol× c(HCl)=6×10-4 mol/0.02 L=3×10-2 mol·L-1
![]() =6×10-4 mol
=6×10-4 mol 练习册系列答案
练习册系列答案
新课标教材同步导练绩优学案系列答案
智慧鸟单元评估卷系列答案
中考必备河南中考试题精选精析卷系列答案
小学英语测试AB卷系列答案
学法大视野单元测试卷系列答案
新领程必考口算应用题系列答案
教材全析系列答案
全优学练测随堂学案系列答案
优加口算题卡系列答案
节节高名师课时计划系列答案
相关题目







