题目内容
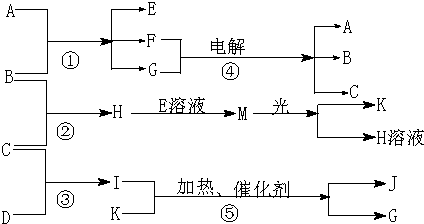
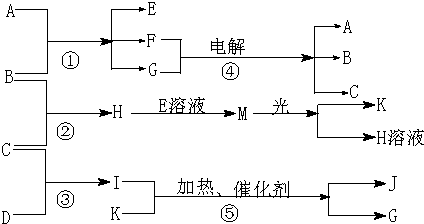
物质A是化合物,B、C、D、K都是单质,反应②~⑤都是常见的工业生产的反应,请填写下列空白:
 ?
?
(1)写出下列物质的化学式:B______; J______.
(2)写出下列反应的离子方程式:
①H+E(溶液)→M______.?
②I溶于G表现碱性______.?
(3)在通常状况下,若1g C气体在B气体中燃烧生成H气体时放出92.3kJ热量,则2molH气体完全分解生成C气体和B气体的热化学方程式为?______.
解:物质A是化合物,B、C、D、K都是单质,反应②~⑤都是常见的工业生产的反应,依据反应条件催化剂加热说明是氨气的催化氧化,所以C+D=I是工业合成氨的反应,判断I为NH3,K为O2,JG是NO和H2O;反应②是两种单质化合生成物质,证明是工业上制氯化氢,C为H2,B为Cl2,则依据电解条件和反应特征判断A为NaOH,E为NaOH,G为H2O,F为NaCl;H(HCl)+E(NaClO)=M可知,M为HClO,见光分解生成K(O2)和H(HCl);
(1)分析推断得到B为Cl2,J为NO,故答案为:Cl2 ;NO;
(2)①H(HCl)+E(NaClO)=M(HClO),反应的离子方程式为:H++ClO-?HClO,故答案为:H++ClO-=HClO;
②I(NH3)溶于G(H2O)表现碱性,是因为案情和水反应生成了一水合氨发生电离,电离出氢氧根离子显碱性,所以原因为NH3+H2O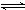 NH3?H2O
NH3?H2O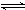 NH4++OH-,
NH4++OH-,
故答案为:NH3+H2O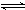 NH3?H2O
NH3?H2O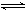 NH4++OH-;
NH4++OH-;
(3)若1g C气体在B气体中燃烧生成H气体时放出92.3kJ热量,则2molH气体完全分解生成C气体和B气体的热化学方程式2HCl(g)=H2(g)+Cl2(g)△H=+184.6 kJ?mol-1,
故答案为:2HCl(g)=H2(g)+Cl2(g)△H=+184.6 kJ?mol-1.
分析:物质A是化合物,B、C、D、K都是单质,反应②~⑤都是常见的工业生产的反应,依据反应条件催化剂加热说明是氨气的催化氧化,所以C+D=I是工业合成氨的反应,判断I为NH3,K为O2,JG是NO和H2O;反应②是两种单质化合生成物质,证明是工业上制氯化氢,C为H2,B为Cl2,则依据电解条件和反应特征判断A为NaOH,E为NaOH,G为H2O,F为NaCl;H(HCl)+E(NaClO)=M可知,M为HClO,见光分解生成K(O2)和H(HCl),所以推断出各物质进行分析回答.
点评:本题考查了物质转化,物质性质的综合应用,主要考查常见的两种单质化合生成物质的工业生产反应,特征化学反应条件的应用,熟悉物质性质是解题关键.
(1)分析推断得到B为Cl2,J为NO,故答案为:Cl2 ;NO;
(2)①H(HCl)+E(NaClO)=M(HClO),反应的离子方程式为:H++ClO-?HClO,故答案为:H++ClO-=HClO;
②I(NH3)溶于G(H2O)表现碱性,是因为案情和水反应生成了一水合氨发生电离,电离出氢氧根离子显碱性,所以原因为NH3+H2O
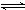 NH3?H2O
NH3?H2O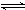 NH4++OH-,
NH4++OH-,故答案为:NH3+H2O
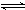 NH3?H2O
NH3?H2O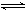 NH4++OH-;
NH4++OH-;(3)若1g C气体在B气体中燃烧生成H气体时放出92.3kJ热量,则2molH气体完全分解生成C气体和B气体的热化学方程式2HCl(g)=H2(g)+Cl2(g)△H=+184.6 kJ?mol-1,
故答案为:2HCl(g)=H2(g)+Cl2(g)△H=+184.6 kJ?mol-1.
分析:物质A是化合物,B、C、D、K都是单质,反应②~⑤都是常见的工业生产的反应,依据反应条件催化剂加热说明是氨气的催化氧化,所以C+D=I是工业合成氨的反应,判断I为NH3,K为O2,JG是NO和H2O;反应②是两种单质化合生成物质,证明是工业上制氯化氢,C为H2,B为Cl2,则依据电解条件和反应特征判断A为NaOH,E为NaOH,G为H2O,F为NaCl;H(HCl)+E(NaClO)=M可知,M为HClO,见光分解生成K(O2)和H(HCl),所以推断出各物质进行分析回答.
点评:本题考查了物质转化,物质性质的综合应用,主要考查常见的两种单质化合生成物质的工业生产反应,特征化学反应条件的应用,熟悉物质性质是解题关键.

练习册系列答案
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
 ?
? NH3?H2O
NH3?H2O NH4++OH-
NH4++OH-