��Ŀ����
����Ŀ��п���仯������;�㷺������п����п��(��Ҫ�ɷ���ZnS)Ϊ��Ҫԭ�ϣ��漰����Ҫ��Ӧ�У�
2ZnS(s)+3O2 (g)=2ZnO(s)+2SO2(g) ��H=-930 kJ��mol-l
C(s)+O2 (g)=CO2 (g) ��H=-393.5 kJ��mol-l
C(s)+CO2 (g)![]() 2CO(g) ��H=+172.5 kJ��mol-l
2CO(g) ��H=+172.5 kJ��mol-l
ZnO(s)+CO(g)=Zn(g)+CO2(g)��H=+198 kJ��mol-l
�ش��������⣺
��1����ӦZnS(s)+C(s)+2O2(g)=Zn(g)+CO2(g)+SO2(g)�� ��H=_______ kJ��mol-l��
��2������п�ɹ㷺����ӡȾýȾ����ľ�ķ�������ZnSO4���ȷֽ�����и����ʵ����ʵ������¶ȱ仯��ϵ��ͼ��ʾ��
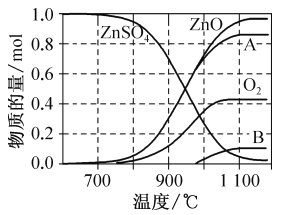
��д��700��980��ʱ������Ӧ�Ļ�ѧ����ʽ��___________������B�Ļ�ѧʽ��_________��
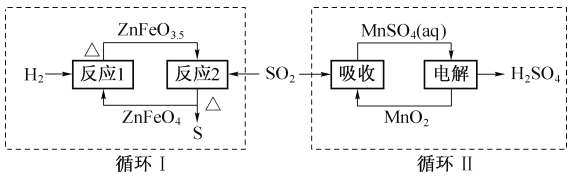
������п�ֽ����ɵ�SO2����ͼ�е�����ѭ���ɷֱ�õ�S��H2SO4��д��ѭ��I�з�Ӧ2�Ļ�ѧ����ʽ��_________��ѭ�����е�����������Ӧʽ��_________��
���𰸡� -377.5 2ZnSO4![]() 2ZnO+2SO2��+O2�� SO3 4ZnFeO3.5+SO2
2ZnO+2SO2��+O2�� SO3 4ZnFeO3.5+SO2![]() 4ZnFeO4 +S Mn2+-2e-+2 H2O =MnO2��+4H+
4ZnFeO4 +S Mn2+-2e-+2 H2O =MnO2��+4H+
����������1����4���Ȼ�ѧ����ʽ���Ϊ��2ZnS(s)+3O2 (g)=2ZnO(s)+2SO2(g) ��H=-930 kJ![]() mol-l��C(s)+O2 (g)=CO2 (g) ��H=-393.5 kJ
mol-l��C(s)+O2 (g)=CO2 (g) ��H=-393.5 kJ![]() mol-l��C(s)+CO2 (g)
mol-l��C(s)+CO2 (g)![]() 2CO(g) ��H=+172.5 kJ
2CO(g) ��H=+172.5 kJ![]() mol-l��ZnO(s)+CO(g)=Zn(g)+CO2 (g) ��H=+198 kJ
mol-l��ZnO(s)+CO(g)=Zn(g)+CO2 (g) ��H=+198 kJ![]() mol-l������
mol-l������![]() +��
+��![]() +��
+��![]() +���ɵ�ZnS(s)+C(s)+2O2(g)=Zn(g)+CO2(g)+SO2(g)��������H=��-930 kJ
+���ɵ�ZnS(s)+C(s)+2O2(g)=Zn(g)+CO2(g)+SO2(g)��������H=��-930 kJ![]() mol-l��
mol-l��![]() +��-393.5 kJ
+��-393.5 kJ![]() mol-l��
mol-l��![]() +��+172.5 kJ
+��+172.5 kJ![]() mol-l��
mol-l��![]() +��+198 kJ
+��+198 kJ![]() mol-l��= -377.5 kJ
mol-l��= -377.5 kJ![]() mol-l��
mol-l��
��2������ͼ���֪��700��980��ʱ��������A��ZnO�����ʵ�����ͬ��ͬʱ������O2������AΪSO2��������Ӧ�Ļ�ѧ����ʽ��2ZnSO4![]() 2ZnO+2SO2��+O2�������¶ȸ���980��ʱ������A�����ʵ���С��ZnO����S�غ��֪������B�Ļ�ѧʽ��SO3 ��
2ZnO+2SO2��+O2�������¶ȸ���980��ʱ������A�����ʵ���С��ZnO����S�غ��֪������B�Ļ�ѧʽ��SO3 ��
������п�ֽ����ɵ�SO2����ͼ�е�����ѭ���ɷֱ�õ�S��H2SO4����ͼ��֪��ѭ��I�з�Ӧ1�� ZnFeO4��������ԭ��2ZnFeO4+H2=2ZnFeO3.5+H2O������Ӧ2�� ZnFeO3.5��SO2��������ѧ����ʽΪ4ZnFeO3.5+SO2![]() 4ZnFeO4 +S��ѭ�����е�����������Ӧʽ��Mn2+-2e-+2 H2O =MnO2��+4H+��
4ZnFeO4 +S��ѭ�����е�����������Ӧʽ��Mn2+-2e-+2 H2O =MnO2��+4H+��