题目内容
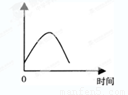
把镁条投入到盛有盐酸的敞口容器里,产生H2的速率可由下图表示,在下列因素中,影响反应速率的是( )
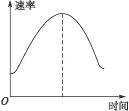
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①②③ D.②③
C
解析:
镁条和盐酸反应产生H2的反应方程式为:Mg+2H+====Mg2++H2↑,是镁与酸中的H+间的置换反应,与Cl-无关,故④不是影响该反应速率的因素。
在镁条的表面有一层氧化膜。当将镁条投入盐酸中时,随着氧化膜的不断溶解,Mg与盐酸接触面积不断增大,则产生的H2的速率会加快。溶液的温度对该反应也有影响,温度越高,产生H2的速率越快。随着反应的进行,H+浓度不断减小,则反应速率会逐渐减慢,故答案为C。

练习册系列答案
相关题目
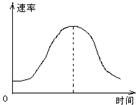 把镁条投入到盛有盐酸的敞口容器里,产生H2的速率可由右图表示.在下列因素中:①盐酸的浓度;②镁条的表面积;③溶液的温度;④Cl-的浓度.影响反应速率的因素是( )
把镁条投入到盛有盐酸的敞口容器里,产生H2的速率可由右图表示.在下列因素中:①盐酸的浓度;②镁条的表面积;③溶液的温度;④Cl-的浓度.影响反应速率的因素是( )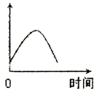
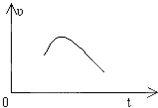 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的主要因素是( )
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的主要因素是( )