题目内容
NA表示表示阿伏伽德罗常数的值,下列说法正确的是
| A.1mol Na2O2粉末中含离子总数为4NA |
| B.22.4LCO2中含有的原子数为3NA |
| C.1mol单质钠在常温下或点燃条件下与O2完全反应转移的电子数都为NA |
| D.在一定量的稀硝酸中加入56g铁粉且完全溶解,转移的电子一定为3NA |
C
解析试题分析:A、1mol Na2O2粉末中含离子总数为3NA,错误;B、没说明状况,错误;C、正确;D、当铁粉过量时,转移的电子就比3NA少,错误。
考点:考查物质的量。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是
| A.1.00mol NaCl中含有6.02×1023个NaCl分子 |
| B.1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |
| C.欲配制1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠 |
有氧化铜和氧化铁的混合物a g,加入2 mol·L-1的硫酸溶液50 mL,恰好完全溶解,若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为
| A.1.6 a g | B.(a-1.6)g | C.(a-3.2)g | D.无法计算 |
下列说法中正确的是( )
①1 mol O2的质量是32 g·mol-1 ②H2的摩尔质量是2 g ③1 mol H+的质量是1 g
④对原子而言,摩尔质量就是相对原子质量
| A.①②③ | B.③④ | C.③ | D.②④ |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.2.4g金属镁变为镁离子时失去的电子数为0.2NA |
| B.1mo1·L-1的A1C13溶液中,C1-离子的数目为3 NA |
| C.标准状况下,11.2LH2O含有的分子数为0.5NA |
| D.常温常压下,32g O2和O3的混合气体所含原子数为2.5NA |
咖啡因(化学式为C8H10N4O2)能兴奋中枢神经、消除疲劳。(1)咖啡因属那一类别的物质 (填“有机物”或“无机物”)其摩尔质量为 .(2)若一杯咖啡含0.194克咖啡因那这杯咖啡中有 个咖啡分子。
下列化学用语使用正确的是
A.Mg2+结构示意图: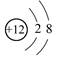 |
B.含18个中子的氯原子的核素符号: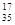 Cl Cl |
C.NH4Cl的电子式: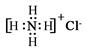 |
D.四氯化碳分子球棍模型: |
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
| A.两种气体的压强相等 | B.O2比O3质量小 |
| C.两种气体的分子数目相等 | D.两种气体的氧原子数目相等 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.0.2mol铁粉与足量水蒸气反应生成的H2分子数为0.3NA |
| B.常温常压下,0.1mol Na2O2与CO2完全反应转移电子数为0.1NA |
| C.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D.某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |