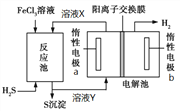
��Ŀ����
����Ŀ������Ļ��������Ź㷺����;����ش��������⣺
��1������Ԫ�����ڱ��е�λ��Ϊ_________�������Ų�ʽ��________����Ԫ����������Ȼͬλ��10B��11B����Ԫ�صĽ������ԭ������Ϊ10.8��������ͬλ��ԭ�ӵ�ԭ�Ӹ���֮��Ϊ_______��
��2��������B����һ����������NaOH��Һ��Ӧ����NaBO2��һ�����壬��д���÷�Ӧ�Ļ�ѧ����ʽ________________��
��3�����ᣨH3BO3����һ�ְ�ɫƬ״���壬����ˮ���������������֯���źͻ��ķ����������á�������һԪ���ᣬ����ʱ0.1mol/L�����pHΪ5����������ĵ��볣��K��__________�������ᣨHBF4����һ��ǿ�ᣬ��������״̬������ˮ�У���д��BF4���ĵ���ʽ__________��
��4��B2H6�����һ����̬�⻯�����������飨C2H6�����ƶ�����Ϊ�����顣
�پ��ⶨB2H6��Bԭ�������Ҳ����8���ӽṹ���ɴ��Ʋ�B2H6��C2H6���ӽṹ_________�����ͬ������ͬ������
��B2H6����BF3��NaBH4��һ�������·�Ӧ�Ƶã�д���÷�Ӧ�Ļ�ѧ����ʽ_________��
��B2H6��ǿ��ԭ��������ˮ��Ӧ����H3BO3��H2������0.1mol B2H6��ˮ��ȫ��Ӧ�������H2�ڱ�״���µ����Ϊ_________L��
���𰸡� �ڶ�����IIIA�� 1s22s22p1 1:4 2B + 2NaOH + 2H2O =2 NaBO2 + 3H2 �� 10-9  ����ͬ BF3 + 3NaBH4 = 2B2H6 +3 NaF 13.44
����ͬ BF3 + 3NaBH4 = 2B2H6 +3 NaF 13.44
����������1������Ԫ�����ڱ��е�λ��Ϊ�ڶ�����IIIA�壬�����Ų�ʽ��1s22s22p1����Ԫ����������Ȼͬλ��10B��11B����Ԫ�صĽ������ԭ������Ϊ10.8��BԪ�ص����ԭ������10.8���������ֱ�Ϊ10��11�ĺ��ص�ƽ��ֵ�����Բ���ʮ�ֽ��淨��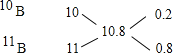 ������10B��11B��ԭ�ӵĸ�����Ϊ0.2��0.8=1��4
������10B��11B��ԭ�ӵĸ�����Ϊ0.2��0.8=1��4
��2��������B����һ����������NaOH��Һ��Ӧ����NaBO2��һ�����壬��д���÷�Ӧ�Ļ�ѧ����ʽ2B + 2NaOH + 2H2O =2 NaBO2 + 3H2 �� ��
��3�����ᣨH3BO3����һ�ְ�ɫƬ״���壬����ˮ���������������֯���źͻ��ķ����������á�������һԪ���ᣬ����ʱ0.1mol/L�����pHΪ5��B(OH)3 +H2O=B(OH)4-+H������������ĵ��볣��K��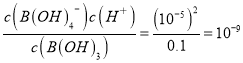 �������ᣨHBF4����һ��ǿ�ᣬ��������״̬������ˮ�У���д��BF4���ĵ���ʽ
�������ᣨHBF4����һ��ǿ�ᣬ��������״̬������ˮ�У���д��BF4���ĵ���ʽ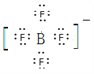 ��
��
��4��B2H6�����һ����̬�⻯�����������飨C2H6�����ƶ�����Ϊ�����顣
�پ��ⶨB2H6��Bԭ�������Ҳ����8���ӽṹ���ɴ��Ʋ�B2H6��C2H6���ӽṹ����ͬ��ÿ����ԭ�Ӿ�Ϊsp3�ӻ���2����ԭ����4����ԭ���γ���ͨ�����������ĸ�������ͬһƽ����,����������ԭ�Ӻ���������ԭ���γ���������ֱ�ڸ�ƽ������ż���Ҳ��Ϊ�����������Ӽ����������̼ԭ�Ӿ�Ϊsp3�ӻ���2��̼ԭ����6����ԭ���γ���ͨ��������2 ��̼֮���γ�һ����������ͼ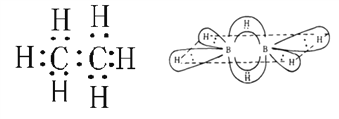 ��
��
��B2H6����BF3��NaBH4��һ�������·�Ӧ�Ƶã��÷�Ӧ�Ļ�ѧ����ʽBF3 + 3NaBH4 = 2B2H6 +3 NaF ��
��B2H6+6H2O��2H3BO3+6H2�� ��0.1mol B2H6��ˮ��ȫ��Ӧ�������0.06molH2�ڱ�״���µ����Ϊ0.06mol*22.4mol/L=13.44L.

 ����˼ά�żӿ���ϵ�д�
����˼ά�żӿ���ϵ�д� �����Ծ�ϵ�д�
�����Ծ�ϵ�д�����Ŀ������ͬ���ܱ������У��øߴ�������Cu2O�ֱ���д��ֽ�ˮ��ʵ�飺2 H2O(g)![]() 2 H2(g) + O2(g) H>0��ʵ���÷�Ӧ��ϵ��ˮ����Ũ�ȣ�mol��L-1���ı仯������£�
2 H2(g) + O2(g) H>0��ʵ���÷�Ӧ��ϵ��ˮ����Ũ�ȣ�mol��L-1���ı仯������£�
��� | ʱ��/min | 0 | 10 | 20 | 30 | 40 | 60 |
�� | �¶�T1 / 1��Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
�� | �¶�T1 / 2��Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
�� | �¶�T2 / 2��Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
����˵������ȷ���ǣ� ��
A. ʵ��ʱ���¶�T2����T1
B. 2��Cu2O�Ĵ�Ч�ʱ�1��Cu2O�Ĵ�Ч�ʸ�
C. ʵ���ǰ20 min��ƽ����Ӧ����v(O2) = 7��10��5 mol��L��1��min��1
D. ����������Cu2O����Cu2O��Ч�ʸߣ�����Cu2O��������С�й�
����Ŀ��ij���������ʵ��̽��SO2�����ʡ�

ʵ������B���������ɣ�C���а�ɫ������D����Һ��ɫ��dz��E�в�����ɫ������
(1)����R��������______________________��
(2)ʵ�����ڳ�������80%���������������Ʒ�ĩ��Ӧ�Ʊ�SO2��д��A�з�Ӧ�Ļ�ѧ����ʽ��______________________________________��
(3)����ʵ�鲽�����£�����װ�á���������ԡ�װҩƷ����װ����ͨ��һ��ʱ��N2��Ȼ������A�з�Ӧ����ͨ��һ��ʱ���N2����Ŀ����___________________________��
(4)̽��װ��C��ͨ��SO2���������Ĺ�ϵ��
������������²��룺
����1��ͨ�������SO2��������Ӧ�����ӷ���ʽΪBa2++2NO3-+3SO2+2H2O=BaSO4�� +2SO42-+2NO+4H+��
����2��ͨ��������SO2��������Ӧ�����ӷ���ʽΪ______________________��
��������������ʵ��֤������1�Ͳ���2�ĸ��������������ʵ�飺
�ṩ�Լ�����ˮ��ͭ�ۡ�Ba(NO3)2��Һ��BaCl2��Һ��Na2CO3��Һ
ʵ�鲽�� | ʵ�������� |
ȡ����C�з�Ӧ����Һ���Թ��У�__________ | ________________ |
(5)���пɼ���װ��D��Ӧ����Һ���Ƿ���Fe2+������Լ���_____(����ĸ)��
a.KSCN��Һ b.NaOH��Һ c.K3[Fe(CN)6]��Һ d.KSCN��Һ��˫��ˮ
(6)�����£�ʵ����Ϻ��롢�ᴿװ��E�а�ɫ����M��ȡ����M���Թ��У�����������(Mʣ��)��������Һ��pH_____7(�>����<����=��)��