题目内容
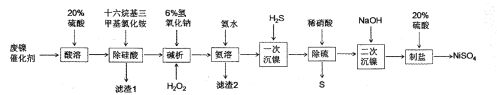
【题目】利用某废镍催化剂(含NiCO3、Na2SiO3,少量Fe3O4、Cr2O3)制备NiSO4,流程如下:
![]()
(1)“酸溶”后,加入十六烷基三甲基氯化铵溶液出现大量白色沉淀,写出“酸溶”时生成硅酸的离子方程式:_________________。
(2)“碱析”时,常温下调pH=____时Fe3+恰好沉淀完全;工业上把pH调至10,此时沉淀物有Fe(OH)3和____,目的是_________。
(3)取300mL“除硅酸”后的溶液,加入双氧水受热th,得到关于沉淀率的关系图如下。
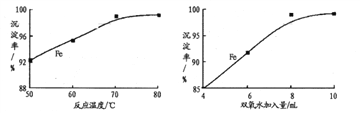
①合适的工艺条件为____________;
②温度不能太高的原因是____。
(4)“一次沉镍”产物为NiS,稀硝酸与之反应的化学反应方程式为____。
【答案】 2H+ + SiO32- = H2SiO3(胶体) 3.2 Ni(OH)2 把Cr3+转化为CrO2-,除去铬元素 70℃ 每300mL加入8mL双氧水 70℃以后沉淀率增加不大,同时双氧水分解速率加快,增加了成本 3NiS + 8HNO3 = 2NO↑ + 4H2O + 3Ni(NO3)2 + 3S↓
【解析】分析:废镍催化剂加入硫酸酸溶后碳酸镍转化为硫酸镍,硅酸钠转化为硅酸,四氧化三铁转化为硫酸铁、硫酸亚铁,Cr2O3转化为硫酸铬,加入双氧水将亚铁离子氧化为铁离子,加入氢氧化钠沉淀铁离子。根据已知信息可知加入氨水沉淀铬离子,利用H2S沉淀镍离子,利用硝酸的氧化性除去硫,然后再利用氢氧化钠沉淀镍离子,最后用硫酸溶解得到硫酸镍,据此解答。
详解:(1)“酸溶”后,加入十六烷基三甲基氯化铵溶液出现大量白色沉淀,这说明“酸溶”时生成的是硅酸胶体,所以“酸溶”时生成硅酸的离子方程式为2H+ +SiO32-=H2SiO3(胶体)。
(2)根据氢氧化铁的溶度积常数可知铁离子恰好沉淀时溶液中氢氧根的浓度是![]() ,则溶液的pH=3.2;由于氢氧化铬的性质类似于氢氧化铝,则当氢氧化钠过量时会生成NaCrO2,因此工业上把pH调至10,此时沉淀物有Fe(OH)3和Ni(OH)2,目的是把Cr3+转化为CrO2-,除去铬元素。
,则溶液的pH=3.2;由于氢氧化铬的性质类似于氢氧化铝,则当氢氧化钠过量时会生成NaCrO2,因此工业上把pH调至10,此时沉淀物有Fe(OH)3和Ni(OH)2,目的是把Cr3+转化为CrO2-,除去铬元素。
(3)①根据图像可知温度为70℃、加入8mL双氧水时沉淀率高,因此合适的工艺条件为70℃、每300mL加入8mL双氧水;
②由于70℃以后沉淀率增加不大,同时双氧水分解速率加快,增加了成本,所以温度不能太高。
(4)“一次沉镍”产物为NiS,由于硝酸具有氧化性,则稀硝酸与之反应的化学反应方程式为3NiS+8HNO3=2NO↑+4H2O+3Ni(NO3)2+3S↓。

