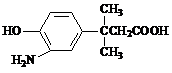题目内容
(08年江苏卷)(10分)工业上制备BaCl2的工艺流程图如下:

某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得:
BaSO4(s) + 4C(s)![]() 4CO(g) + BaS(s) △H1 = 571.2 kJ?mol-1 ①
4CO(g) + BaS(s) △H1 = 571.2 kJ?mol-1 ①
BaSO4(s) + 2C(s)![]() 2CO2(g) + BaS(s) △H2= 226.2 kJ?mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ?mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g)![]() 2CO(g)的△H2= kJ?mol-1。
2CO(g)的△H2= kJ?mol-1。
⑷实际生产中必须加入过量的炭,同时还要通入空气,其目的是
答案:⑴S2- + H2O![]() HS- +OH- HS- + H2O
HS- +OH- HS- + H2O![]() H2S +OH-(可不写)
H2S +OH-(可不写)
⑵2.7×10-3
⑶172.5
⑷使BaSO4得到充分的还原(或提高BaS的产量)
①②为吸热反应,炭和氧气反应放热维持反应所需高温
解析:Na2S水解实际上是二元弱酸根S2水解,因分两步,向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,两种沉淀的平衡体系中银离子浓度是一样的, =[Ksp(AgBr) /Ksp(AgCl) =2.7×10-3, 反应C(s) + CO2(g)
=[Ksp(AgBr) /Ksp(AgCl) =2.7×10-3, 反应C(s) + CO2(g)![]() 2CO(g)的△H3等于△H1减去△H2。实际生产中必须加入过量的炭,同时还要通入空气,其目的是炭和氧气反应放热维持反应所需高温来维持反应①②所需热量。
2CO(g)的△H3等于△H1减去△H2。实际生产中必须加入过量的炭,同时还要通入空气,其目的是炭和氧气反应放热维持反应所需高温来维持反应①②所需热量。

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 Ag++2CN - == [Ag(CN)2] -
Ag++2CN - == [Ag(CN)2] -
 b.
b. c.
c. d.
d.
 b.
b.
 d.
d.