题目内容
在H2S![]() H++HS-,HS-
H++HS-,HS-![]() H++S2-的电离平衡中,由于条件的改变,下列浓度是怎样变化的?[填“变大”,“变小”或“不变”]
H++S2-的电离平衡中,由于条件的改变,下列浓度是怎样变化的?[填“变大”,“变小”或“不变”]
(1)加入稀H2SO4,则[S2-]________,[H+]________.
(2)加入CuSO4,则[H2S]________,[S2-]________.
(3)加入少量水,则[S2-]________,[H+]________.
(4)加入少量NaOH,则[S2-]________,[H+]________.
(5)滴入少量氯水,则[S2-]________,[H+]________.
(6)通入适量SO2,则[H2S]________,[H+]________.
(7)加入少量Mg粉,则[H2S]________,[H+]________.
(8)加热煮沸一会儿,则[H2S]________,[H+]________.
答案:
解析:
解析:
|
(1)变小,变大;(2)变小,变小;(3)变小,变小;(4)变大,变小;(5)变小,变大;(6)变小,变小;(7)变小,变小;(8)变小,变小 导解:运用化学平衡移动原理进行判断. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
|
硫化氢的水溶液中有如下动态平衡: H2S 在物质的量浓度为0.1 mol·L-1的H2S溶液中,下列各离子间的关系正确的是 | |
| [ ] | |
A. |
c (H+)=c(HS-)+2c(S2-)+c(OH-) |
B. |
2c(H+)=2c(HS-)+c(S2-)+2c(OH-) |
C. |
c (H+)=c(HS-)+2c(S2-) |
D. |
c (H+)=2c(S2-)+c(OH-) |
 H++HS-;HS-
H++HS-;HS-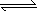 H++S2-;H2O
H++S2-;H2O H++OH-
H++OH-