题目内容
设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.0.5 L 1 mol/L NaHS溶液中,N(Na+)+N(HS—)=NA |
| B.12.4 g白磷(分子式为P4)中含有P—P共价键0.6 NA |
| C.常温下,pH=2的醋酸溶液中所含有的H+数为0.01 NA |
| D.将92 g N2O4晶体放入容器中,恢复到常温常压时,所含气体分子数为NA |
B
解析试题分析:A、在0.5mol的NaHS中Na+和HS-的个数共1mol,但在溶液中HS-离子会发生电离和水解,故HS-的个数减少,N(Na+)+N(HS)的总数小于NA,故A错误;B、白磷是正四面体结构,一个白磷分子中含6条P-P键,白磷0.1mol,故P-P键的数目为0.6NA,故B正确;C、没溶液的体积,不能求出溶液中氢离子的个数,故C错误;D、在容器中存在N2O4=2NO2的可逆反应,故放入容器中因发生该反应而使气体分子数增多,故D错误;故选B。
考点:微粒数目的计算。

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
| A.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5 NA |
| B.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移电子总数为0.2 NA |
| C.1.8 g重水(D2O)中含NA个中子 |
| D.足量的铜与含2 mol H2SO4的浓硫酸充分反应,可生成NA个SO2分子 |
阿伏加德罗常数约为6.02×1023 mol-1,下列说法中正确的是
| A.4 g重水(D2O)中所含质子数为0.2×6.02×1023 |
| B.4.48 L N2与CO的混合物所含分子数为0.2×6.02×1023 |
| C.6.2 g白磷与红磷的混合物中所含磷原子数为0.2×6.02×1023 |
| D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2×6.02×1023 |
下列化学用语表示正确的是
| A.原子核中有6个中子的硼原子:6B | B.HCl的电子式: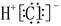 |
C.K+结构示意图: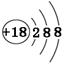 | D.HClO的结构式:H—O—Cl |
下列有关化学用语表示正确的是
A.四氯化碳分子比例模型:  | B.COS的电子式是 |
| C.次氯酸的结构式为 H-Cl-O | D. O2-离子结构示意图: O2-离子结构示意图: |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.1mol Na与乙醇完全反应,失去2nA电子 |
| B.常温常压下,10gCH4含有10nA个电子 |
| C.1L 0.1mol?L-1的醋酸溶液中含有0.1nA个H+ |
| D.标准状况下,22.4L苯含有nA个苯分子 |
同温同压下某瓶充满O2时重116g,充满CO2时重122g,充满某气体时重132g,则该未知气体的相对分子质量为( )
| A.28 | B.64 | C.32 | D.44 |
设阿伏加德罗常数的值为NA,则下列说法正确的是
| A.标准状况下,11.2L CCl4所含的分子数为0.5NA |
| B.常温常压下,4.2g C2H4和C8H16的混合物中含有的碳原子数为0.3NA |
| C.7.8g苯分子中碳碳双键的数目为0.3 NA |
| D.6.4gCu与20mL10 mol·L-1浓硫酸反应,转移的电子数为0.2NA |
下列关于同温同压下的两种气体12C18O和14N2的判断正确的是( )
| A.体积相等时密度相等 | B.原子数相等时具有的中子数相等 |
| C.体积相等时具有的电子数相等 | D.质量相等时具有的质子数相等 |