题目内容
(I)滴定分析法是化学分析法中的重要分析方法之一.(一)用酸碱中和滴定法测定市售白醋的总酸量(g/100mL).
A.实验步骤:
(1)用酸式滴定管量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL容量瓶中定容,摇匀即得待测白醋溶液.
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴酚酞作指示剂.
(3)读取盛装0.1000mol/L NaOH 溶液的碱式滴定管的初始读数.如果液面位置如图所示,则此时的读数为______.
(4)滴定.当______时,
停止滴定,并记录NaOH溶液的终读数.重复滴定3次.
B.实验记录
| 滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(1)经计算,市售白醋总酸量=______g/100mL.
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是______(填写序号).
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前无气泡,滴定后有气泡
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
(二)用双指示剂法测定纯碱的含量
如图的滴定曲线表示:用0.1000mol/L HCl滴定 20.00ml 0.1000mol/L Na2CO3

①A处选用______作指示剂比较合适;
②当滴定至混合液pH接近4时,为了防止终点出现过早,减少实验误差,应剧烈摇动溶液或加热一会溶液,冷却后再继续滴定,这样做的理由是:______.
(II)由于MnO2能作H2O2溶液分解的催化剂,某校化学兴趣小组想探究其他一些金属氧物质是否也可以作H2O2溶液分解的催化剂?探究过程如下.
(1)[猜想]:Al2O3能作过氧化氢分解的催化剂.
(2)[实验验证]:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中 | 木条不复燃 | 常温下过氧化氢溶液不分解(或分解很少)______ |
| 实验二 | 在装有H2O2溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 木条复燃 | ______ |
(4)[讨论与反思]:有的同学认为只有上述两个实验,不能完全证明Al2O3在H2O2溶液分解中起了催化作用.还应补充实验来验证:______.
(5)另外化学兴趣小组为比较Fe3+和Cu2+对H2O2分解的催化效果,该组同学设计了如图所示的实验.可通过观察反应产生气泡快慢或反应完成的先后或试管壁的冷热程度定性比较得出结论.有同学提出将CuSO4改为CuCl2更为合理,其理由是______,你认为还可以作何改进?______.


【答案】分析:(I)(一)(3)根据滴定管的结构和精确度来解答;
(4)根据滴定终点,溶液由无色恰好变为红色,且半分钟内不褪色,停止滴定;
C.(1)先根据数据的有效性,舍去第1组数据,然后求出2、3、4三组平均消耗V(NaOH),接着根据醋酸和NaOH反应求出20.00mL样品中含有的醋酸,最后求出市售白醋总酸量;
(2)根据c(待测)=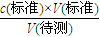 分析误差;
分析误差;
(二)(1)①A处在碱性条件下变色;
②溶液中含有H2CO3;
(II)(2)实验二:Al2O3能加快H2O2溶液的分解速率;
(4)根据催化剂的质量和化学性质在反应前后不变;
(5)阴离子也能影响化学反应速率;将FeCl3改为Fe2(SO4)3;
解答:解:(I)(一)(3)液面读数0.70mL,故答案为:0.70mL;
(4)滴定终点时,溶液由无色恰好变为红色,且半分钟内不褪色,停止滴定,故答案为:溶液由无色恰好变为红色,且半分钟内不褪色;
C.(1)C.(1)先根据数据的有效性,舍去第1组数据,然后求出2、3、4三组平均消耗V(NaOH)=15.00mL,
CH3COOH+NaOH=CH3COONa+H2O
0.0015mol 0.015L×0.1000mol/L
则20.00mL样品中含有的醋酸的质量为0.0015mol×60g/mol=0.9g,市售白醋总酸量4.5g/100mL;
(2)a.碱式滴定管在滴定时未用标准NaOH溶液润洗,会使得标准NaOH溶液浓度减小,造成V(标准)偏大,根据c(待测)=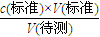 分析误差 可知c(标准)偏大,故a正确;
分析误差 可知c(标准)偏大,故a正确;
b.碱式滴定管的尖嘴在滴定前无气泡,滴定后有气泡,造成V(标准)偏小,根据c(待测)=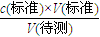 分析误差 可知c(标准)偏小,故b错误;
分析误差 可知c(标准)偏小,故b错误;
c.锥形瓶中加入待测白醋溶液后,再加少量水,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=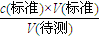 分析误差 可知c(标准)不变,故c错误;
分析误差 可知c(标准)不变,故c错误;
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出,待测液的物质的量减小,造成V(标准)减小,根据c(待测)=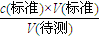 分析误差 可知c(标准)偏小,故d错误;
分析误差 可知c(标准)偏小,故d错误;
故选:a;
(二)(1)①A处在碱性条件下变色,所以选用酚酞,故答案为:酚酞;
②溶液中含有H2CO3,加热或振荡加快H2CO3的分解,除去溶液中过多的CO2;故答案为:加快H2CO3的分解,除去溶液中过多的CO2;
(II)(2)实验二:Al2O3能加快H2O2溶液的分解速率;故答案为:Al2O3能加快H2O2溶液的分解速率;
(4)上述反应前后Al2O3质量和化学性质是否改变,故答案为:上述反应前后Al2O3质量和化学性质是否改变;
(5)阴离子也能影响化学反应速率,所以控制阴离子相同,排除阴离子的干扰,将FeCl3改为Fe2(SO4)3,故答案为:控制阴离子相同,排除阴离子的干扰;将FeCl3改为Fe2(SO4)3.
点评:本题是一道综合性题目,涉及到的知识点较多,根据所学知识可完成,难度中等.
(4)根据滴定终点,溶液由无色恰好变为红色,且半分钟内不褪色,停止滴定;
C.(1)先根据数据的有效性,舍去第1组数据,然后求出2、3、4三组平均消耗V(NaOH),接着根据醋酸和NaOH反应求出20.00mL样品中含有的醋酸,最后求出市售白醋总酸量;
(2)根据c(待测)=
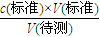 分析误差;
分析误差;(二)(1)①A处在碱性条件下变色;
②溶液中含有H2CO3;
(II)(2)实验二:Al2O3能加快H2O2溶液的分解速率;
(4)根据催化剂的质量和化学性质在反应前后不变;
(5)阴离子也能影响化学反应速率;将FeCl3改为Fe2(SO4)3;
解答:解:(I)(一)(3)液面读数0.70mL,故答案为:0.70mL;
(4)滴定终点时,溶液由无色恰好变为红色,且半分钟内不褪色,停止滴定,故答案为:溶液由无色恰好变为红色,且半分钟内不褪色;
C.(1)C.(1)先根据数据的有效性,舍去第1组数据,然后求出2、3、4三组平均消耗V(NaOH)=15.00mL,
CH3COOH+NaOH=CH3COONa+H2O
0.0015mol 0.015L×0.1000mol/L
则20.00mL样品中含有的醋酸的质量为0.0015mol×60g/mol=0.9g,市售白醋总酸量4.5g/100mL;
(2)a.碱式滴定管在滴定时未用标准NaOH溶液润洗,会使得标准NaOH溶液浓度减小,造成V(标准)偏大,根据c(待测)=
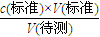 分析误差 可知c(标准)偏大,故a正确;
分析误差 可知c(标准)偏大,故a正确;b.碱式滴定管的尖嘴在滴定前无气泡,滴定后有气泡,造成V(标准)偏小,根据c(待测)=
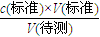 分析误差 可知c(标准)偏小,故b错误;
分析误差 可知c(标准)偏小,故b错误;c.锥形瓶中加入待测白醋溶液后,再加少量水,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=
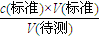 分析误差 可知c(标准)不变,故c错误;
分析误差 可知c(标准)不变,故c错误;d.锥形瓶在滴定时剧烈摇动,有少量液体溅出,待测液的物质的量减小,造成V(标准)减小,根据c(待测)=
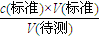 分析误差 可知c(标准)偏小,故d错误;
分析误差 可知c(标准)偏小,故d错误;故选:a;
(二)(1)①A处在碱性条件下变色,所以选用酚酞,故答案为:酚酞;
②溶液中含有H2CO3,加热或振荡加快H2CO3的分解,除去溶液中过多的CO2;故答案为:加快H2CO3的分解,除去溶液中过多的CO2;
(II)(2)实验二:Al2O3能加快H2O2溶液的分解速率;故答案为:Al2O3能加快H2O2溶液的分解速率;
(4)上述反应前后Al2O3质量和化学性质是否改变,故答案为:上述反应前后Al2O3质量和化学性质是否改变;
(5)阴离子也能影响化学反应速率,所以控制阴离子相同,排除阴离子的干扰,将FeCl3改为Fe2(SO4)3,故答案为:控制阴离子相同,排除阴离子的干扰;将FeCl3改为Fe2(SO4)3.
点评:本题是一道综合性题目,涉及到的知识点较多,根据所学知识可完成,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 求出原稀溶液中I-浓度,滴定时的反应为:2Na2S2O3 + I2 = Na2S4O6 + 2NaI。试回答:
求出原稀溶液中I-浓度,滴定时的反应为:2Na2S2O3 + I2 = Na2S4O6 + 2NaI。试回答: ____________(填“是”或“不是”);若为AgX沉淀,则它的化学式为__________(若不为AgX沉淀,则此空不填)。
____________(填“是”或“不是”);若为AgX沉淀,则它的化学式为__________(若不为AgX沉淀,则此空不填)。