题目内容
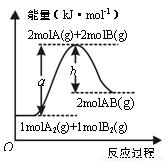
下列反应中,同时符合图像Ⅰ和Ⅱ的是

A.N2(g)+3H2(g)  2NH3(g) ΔH<0
2NH3(g) ΔH<0
B.2SO3(g)  2SO2(g)+O2(g) ΔH>0
2SO2(g)+O2(g) ΔH>0
C.H2(g)+CO(g) 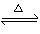 C(s)+H2O(g) ΔH>0
C(s)+H2O(g) ΔH>0
D.4NH3(g)+5O2(g) 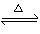 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
D
【解析】
试题分析:A.正反应是放热反应。升高温度,化学反应速率加快,达到平衡所需要的时间缩短。由于该反应的正反应为放热反应。所以当反应达到平衡后,升高温度,平衡逆向移动,生成物的浓度进行。正反应是气体体积减小的反应。增大压强,V正>V逆,平衡正向移动。错误。B.反应2SO3(g)  2SO2(g)+O2(g) ΔH>0的正反应是气体体积增大的吸热反应。在其它条件不变时,升高温度,化学平衡向正反应方向移动,生成物的浓度增大。在其它条件不变时,增大压强,生成物的浓度增大的多,V逆>V正化学平衡向逆反应方向移动。错误。C.H2(g)+CO(g)
2SO2(g)+O2(g) ΔH>0的正反应是气体体积增大的吸热反应。在其它条件不变时,升高温度,化学平衡向正反应方向移动,生成物的浓度增大。在其它条件不变时,增大压强,生成物的浓度增大的多,V逆>V正化学平衡向逆反应方向移动。错误。C.H2(g)+CO(g) 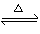 C(s)+H2O(g) ΔH>0该反应的正反应为气体体积减小的吸热反应。在其它条件不变时,升高温度,化学平衡向正反应方向移动,生成物的浓度增大。在其它条件不变时,增大压强,生成物的浓度增大的多,V逆>V正化学平衡向逆反应方向移动。错误。D.反应4NH3(g)+5O2(g)
C(s)+H2O(g) ΔH>0该反应的正反应为气体体积减小的吸热反应。在其它条件不变时,升高温度,化学平衡向正反应方向移动,生成物的浓度增大。在其它条件不变时,增大压强,生成物的浓度增大的多,V逆>V正化学平衡向逆反应方向移动。错误。D.反应4NH3(g)+5O2(g) 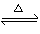 4NO(g)+6H2O(g) ΔH<0的正反应是气体体积增大的放热反应。在其它条件不变时,升高温度,平衡逆向移动,生成物的浓度减小。在其它条件不变时,增大压强,V逆>V正,平衡逆向移动,生成物的浓度减小。正确。
4NO(g)+6H2O(g) ΔH<0的正反应是气体体积增大的放热反应。在其它条件不变时,升高温度,平衡逆向移动,生成物的浓度减小。在其它条件不变时,增大压强,V逆>V正,平衡逆向移动,生成物的浓度减小。正确。
考点:考查温度、压强对化学平衡、生成物的浓度的影响的知识。

KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去。某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响。该实验条件作如下限定:
①所用KMnO4酸性溶液的浓度可选择:0.02 mol·L-1、0.002 mol·L-1;
②所用H2C2O4溶液的浓度可选择:0.2 mol·L-1、0.4 mol·L-1;
③每次实验时KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液的用量均为2mL。
(1)若要探究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成____ 组实验进行对比即可得出结论。
(2)在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得实验数据(从混合振荡均匀开始计时)如下表所示:
KMnO4酸性溶液浓度 (mol·L-1) | 溶液褪色所需时间(min) | |||
第一次 | 第二次 | 第三次 | ||
0.02 | 14 | 13 | 11 | |
0.002 | 6.7 | 6.6 | 6.7 | |
①用0.002 mol/L KMnO4酸性溶液进行实验时,KMnO4的平均反应速率(忽略混合前后溶液体积变化)。
②依据表中数据,不能得出“溶液的褪色所需时间越短,反应速率越快”的结论。某同学设计以下方案,可以直接得出“褪色时间越短,反应的速率越快”结论。
KMnO4酸性溶液 | H2C2O4溶液 | ||
浓度/ mol/L | 体积(ml) | 浓度/ mol/L | 体积(ml) |
0.02 | 2 | b | 4 |
a | 2 | c | 4 |
则表中a= ;b= ;c= 。
(3)草酸电离常数:Ka1=5.9×10-2,Ka2=6.4×10-5。与KMnO4反应时,它将转化为CO2和H2O。
①草酸与酸性高锰酸钾溶液反应的离子方程式为 。
②室温下,0.1mol·L-1 KHC2O4酸溶液中pH 7,理由是 。
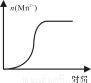
(4)测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图。请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因: 。
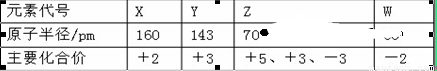
X、Y、Z、W为四种短周期元素,有关这四种元素的说法中一定正确的是( )
元素 | X | Y | Z | W |
原子半径(nm) | 0.077 | 0.075 | 0.102 | 0.099 |
最高正价或最低负价 | +4 | +5 | -2 | -1 |
A.X与W形成XW4时,各原子最外层均满 足8电子稳定结构,
B.1molW的单质参加氧化还原反应时转移的电子数为2mol
C.0.3molCu分别与足量HYO3和H2ZO4的稀溶液反应均产生0.2mol气体
D.Y的氢化物与W的氢化物反应的产物只含有共价键