题目内容
Li2C2,Mg2C3,Al4C3,ZnC2跟CaC2一样,同属离子型碳化物。已知CaC2与H2O可以发生水解反应并生成C2H2,以下判断正确的是( )A.Li2C2水解生成乙烯(C2H4)
B.Mg2C3水解生成丙炔(C3H4)
C.Al4C3水解生成丙炔(C3H4)
D.ZnC2水解生成乙烷(C2H6)
答案:B
解析:
解析:
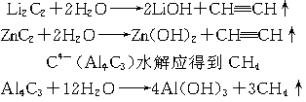
| 解析:(类比法)本题属于信息试题。解答此题首先要理解给出的信息。题中给出的信息有两条:一是几种碳化物跟CaC2一样都是离子型碳化物,二是CaC2水解可得乙炔。因此,首先得弄清CaC2的结构以及它跟水反应的原理。
CaC2是离子型碳化物,就是说它是由Ca2+和C C C Mg2C3+4H2O
|

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目