题目内容
(6分)2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H="–99" kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H="–99" kJ/mol。请回答下列问题:
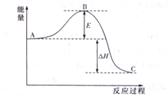
(1)图中E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? 。
(2)写出图中由A生成C的热化学反应方程式 。
(3)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的△H= 。
 2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H="–99" kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H="–99" kJ/mol。请回答下列问题:
(1)图中E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? 。
(2)写出图中由A生成C的热化学反应方程式 。
(3)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的△H= 。
(1)没有影响 降低
(2)2SO2(g)+O2(g) 2SO3(g) △H=-198kJ·mol-1 (其他合理答案均给分)
2SO3(g) △H=-198kJ·mol-1 (其他合理答案均给分)
(3)-1185kJ/mol
(2)2SO2(g)+O2(g)
 2SO3(g) △H=-198kJ·mol-1 (其他合理答案均给分)
2SO3(g) △H=-198kJ·mol-1 (其他合理答案均给分)(3)-1185kJ/mol
(1)根据图像可知E代表的是反应的活化能,不会影响反应热,反应热只与反应物和生成物的能量的相对大小有关。催化剂会降低反应的活化能,从而加快反应速率。
(2)在图中A点表示2mol二氧化硫和1mol氧气,所以反应的热化学方程式为2SO2(g)+O2(g) 2SO3(g) △H=-198kJ·mol-1。
2SO3(g) △H=-198kJ·mol-1。
(3)硫的燃烧热为296 kJ/mol,所以热化学方程式为①S(s)+O2(g)=SO2(g) △H=-296kJ·mol-1.将该反应和反应②2SO2(g)+O2(g) 2SO3(g) △H=-198kJ·mol-1叠加,即①×2+②得到2S(s)+3O2(g)=2SO3(g),所以该反应的△H=-790kJ·mol-1.因此生成3 mol SO3(g)的△H=-1185kJ/mol。
2SO3(g) △H=-198kJ·mol-1叠加,即①×2+②得到2S(s)+3O2(g)=2SO3(g),所以该反应的△H=-790kJ·mol-1.因此生成3 mol SO3(g)的△H=-1185kJ/mol。
(2)在图中A点表示2mol二氧化硫和1mol氧气,所以反应的热化学方程式为2SO2(g)+O2(g)
 2SO3(g) △H=-198kJ·mol-1。
2SO3(g) △H=-198kJ·mol-1。(3)硫的燃烧热为296 kJ/mol,所以热化学方程式为①S(s)+O2(g)=SO2(g) △H=-296kJ·mol-1.将该反应和反应②2SO2(g)+O2(g)
 2SO3(g) △H=-198kJ·mol-1叠加,即①×2+②得到2S(s)+3O2(g)=2SO3(g),所以该反应的△H=-790kJ·mol-1.因此生成3 mol SO3(g)的△H=-1185kJ/mol。
2SO3(g) △H=-198kJ·mol-1叠加,即①×2+②得到2S(s)+3O2(g)=2SO3(g),所以该反应的△H=-790kJ·mol-1.因此生成3 mol SO3(g)的△H=-1185kJ/mol。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目