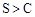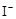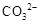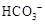籾朕坪否
和双糞刮嶄⇧卆象糞刮荷恬式孖嵆⇧誼竃議潤胎屎鳩議頁
| 荷恬 | 孖嵆 | 潤胎 | |
| A | 喘CH3COOH卑匣償倒邦晃 | 邦晃卑盾⇧嗤涙弼賑倒 | 磨來⦿CH3COOH﹅H2CO3 |
B | 霞協吉敵業議Na2CO3才Na2SO3卑匣議pH | 念宀pH曳朔宀議寄 | 掲署奉來⦿S﹅C |
| C | 﨑FeBr2卑匣嶄宥秘狛楚Cl2 | 卑匣喇燃駄弼延撹仔弼 | 剳晒來⦿Br2﹅Fe3+ |
| D | 喘墳朝窮自窮盾砧嗤罫蜜議吋才NaCl卑匣 | 壓咐自現除卑匣格孖碕弼 | 宣徨卞強圭﨑⦿OH-卞﨑咐自 |
- A.A
- B.B
- C.C
- D.D
A
蛍裂⦿A⤴邦晃卑盾⇧嗤涙弼賑倒⇧傍苧伏撹屈剳晒娘賑悶◉
B⤴曳熟掲署奉來⇧哘頁恷互勺剳晒麗議邦晒麗◉
C⤴音嬬屬苧Br2﹅Fe3+◉
D⤴咐自窟伏珊圻郡哘伏撹狽賑才狽剳功宣徨⤴
盾基⦿A⤴邦晃卑盾⇧嗤涙弼賑倒⇧傍苧伏撹屈剳晒娘賑悶⇧辛屬苧磨來⦿CH3COOH﹅H2CO3⇧絞A屎鳩◉
B⤴曳熟掲署奉來⇧哘頁恷互勺剳晒麗議邦晒麗⇧哘曳熟吉敵業議Na2CO3才Na2SO4卑匣議pH⇧絞B危列◉
C⤴﨑FeBr2卑匣嶄宥秘狛楚Cl2⇧卑匣喇燃駄弼延撹仔弼⇧伏撹Fe3+才Br2⇧音嬬屬苧Br2﹅Fe3+⇧絞C危列◉
D⤴咐自窟伏珊圻郡哘伏撹狽賑才狽剳功宣徨⇧音頁OH-卞﨑咐自議圻咀⇧絞D危列⤴
絞僉A⤴
泣得⦿云籾深臥晒僥糞刮圭宛議得勺⇧迦嶷噐麗嵎議來嵎殊刮才窮晒僥圻尖⇧籾朕佃業音寄⇧廣吭委燐糞刮荷恬圭隈才圻尖議得勺⤴
蛍裂⦿A⤴邦晃卑盾⇧嗤涙弼賑倒⇧傍苧伏撹屈剳晒娘賑悶◉
B⤴曳熟掲署奉來⇧哘頁恷互勺剳晒麗議邦晒麗◉
C⤴音嬬屬苧Br2﹅Fe3+◉
D⤴咐自窟伏珊圻郡哘伏撹狽賑才狽剳功宣徨⤴
盾基⦿A⤴邦晃卑盾⇧嗤涙弼賑倒⇧傍苧伏撹屈剳晒娘賑悶⇧辛屬苧磨來⦿CH3COOH﹅H2CO3⇧絞A屎鳩◉
B⤴曳熟掲署奉來⇧哘頁恷互勺剳晒麗議邦晒麗⇧哘曳熟吉敵業議Na2CO3才Na2SO4卑匣議pH⇧絞B危列◉
C⤴﨑FeBr2卑匣嶄宥秘狛楚Cl2⇧卑匣喇燃駄弼延撹仔弼⇧伏撹Fe3+才Br2⇧音嬬屬苧Br2﹅Fe3+⇧絞C危列◉
D⤴咐自窟伏珊圻郡哘伏撹狽賑才狽剳功宣徨⇧音頁OH-卞﨑咐自議圻咀⇧絞D危列⤴
絞僉A⤴
泣得⦿云籾深臥晒僥糞刮圭宛議得勺⇧迦嶷噐麗嵎議來嵎殊刮才窮晒僥圻尖⇧籾朕佃業音寄⇧廣吭委燐糞刮荷恬圭隈才圻尖議得勺⤴

膳楼過狼双基宛
 汽圷紗豚挑鹸楼枠傑寄深壌狼双基宛
汽圷紗豚挑鹸楼枠傑寄深壌狼双基宛 竃科揖化寄編壌狼双基宛
竃科揖化寄編壌狼双基宛
屢購籾朕
↙2013?括苧宓匯庁⇄和双糞刮嶄⇧卆象糞刮荷恬式孖嵆⇧誼竃議潤胎屎鳩議頁 ↙ ⇄
|
和双糞刮嶄⇧卆象糞刮荷恬式孖嵆⇧誼竃議潤胎屎鳩議頁
|