题目内容
19. 实验室制备环己酮的反应原理:
实验室制备环己酮的反应原理: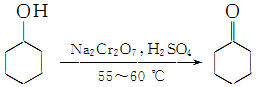 (实验装置如图所示,环己醇、环己酮、饱和食盐水和水的部分物理性质见表).
(实验装置如图所示,环己醇、环己酮、饱和食盐水和水的部分物理性质见表).| 物质 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1 | 0.962 | 能溶于水 |
| 环己酮 | 155.6 | 0.948 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.330 | - |
| 水 | 100.0 | 0.998 | - |
①仪器A的名称是三颈烧瓶
②仪器A中的反应温度应控制在55~60℃,控制温度的方法是55~60℃水浴加热
③蒸馏不能分离环己酮和水的原因是环已酮和水形成具有固定组成的恒沸物一起蒸出
(2)环己酮的提纯需要经过以下一系列的操作:
a.在收集到的粗品中加NaCl固体至饱和,静置,分液
b.加入无水MgSO4固体
c.抽滤
d.蒸馏,收集151~156℃馏分,得到精品
①在反应装置图中牛角管上的支管的作用是与大气连通,保持内外压强一致
②加入无水MgSO4固体的作用是去除有机物中水分
③抽滤需要使用的仪器为抽气泵、吸气瓶、布氏漏斗.
分析 (1)①根据仪器的构造和特点来回答;
②利用酒精灯直接加热不易控制温度,通常加热温度低于100℃时采用水浴加热的方式;
③根据环己酮和水形成的具有固定组成的混合物的沸点和水的沸点相近来回答;
(2)环己酮的提纯时应首先加入NaCl固体,使水溶液的密度增大,将水与有机物更容易分离开来,然后向有机层中加入无水MgSO4,除去有机物中少量的水,然后过滤,除去硫酸镁晶体,再进行蒸馏即可;
①牛角管上的支管与外界想通,可平衡大气压强;
②无水MgSO4易水结合生成结晶水合物;
③抽滤操作需要的仪器是减压系统、布氏漏斗及吸滤瓶.
解答 解:(1)①仪器A的名称是三颈烧瓶,故答案为:三颈烧瓶;
②仪器A中的反应温度应控制在55~60℃,不能直接用酒精灯加热,通常用55~60℃水浴加热方法来控制温度,
故答案为:55~60℃水浴加热;
③环己酮和水能形成具有固定组成的混合物,具有固定的沸点,蒸馏时能被一起蒸出,所以蒸馏难以分离环己酮和水的混合物.环己酮和水能够产生共沸,采取蒸馏是不可取的,建议采用精馏,
故答案为:环已酮和水形成具有固定组成的恒沸物一起蒸出;
(2)①装置图中牛角管上的支管与外界想通,其作用是保持内外压强一致,
故答案为:与大气连通,保持内外压强一致;
②加入无水MgSO4固体,通过生成MgSO4晶体,去除有机物中水分,
故答案为:去除有机物中水分;
③抽滤操作需要的仪器除减压系统外,还需布氏漏斗及吸滤瓶,故答案为:布氏漏斗.
点评 本题通过制取制备环己酮的工艺流程,考查了物质制备方案的设计,题目难度中等,理解工艺流程图、明确实验操作与设计及相关物质的性质是解答本题的关键,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
20.下列物质互为同分异构体的一组是( )
| A. | ${\;}_{\;}^{35}$Cl和${\;}_{\;}^{37}$Cl | B. | H2O和H2O2 | ||
| C. | O2和O3 | D. | CH3CH2OH和CH3OCH3 |
1. 将漫射光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上,如图.下列现象描述正确的是( )
将漫射光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上,如图.下列现象描述正确的是( )
①试管内黄绿色气体逐渐消失;②试管内液面上升;③试管内有油状液体生成;④试管中有少量白雾.
 将漫射光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上,如图.下列现象描述正确的是( )
将漫射光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上,如图.下列现象描述正确的是( )①试管内黄绿色气体逐渐消失;②试管内液面上升;③试管内有油状液体生成;④试管中有少量白雾.
| A. | 只有①② | B. | 只有①③ | C. | 只有①②③ | D. | 全部 |
14. 如图所示装置,可观察到电流计指针偏转,M棒变粗,N棒变细.表所列M、N、P物质中,可以组合成该装置的是( )
如图所示装置,可观察到电流计指针偏转,M棒变粗,N棒变细.表所列M、N、P物质中,可以组合成该装置的是( )
 如图所示装置,可观察到电流计指针偏转,M棒变粗,N棒变细.表所列M、N、P物质中,可以组合成该装置的是( )
如图所示装置,可观察到电流计指针偏转,M棒变粗,N棒变细.表所列M、N、P物质中,可以组合成该装置的是( )| A | B | C | D | |
| M | 锌 | 铜 | 银 | 锌 |
| N | 铜 | 铁 | 锌 | 铁 |
| P | 稀H2SO4 | 稀盐酸 | AgNO3溶液 | Fe(NO3)3溶液 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
4.下列关于有机物的说法中正确的是( )
| A. | 汽油、柴油、植物油都是烃的衍生物 | |
| B. | 米酒变酸的过程涉及了氧化反应 | |
| C. | 含5个碳原子的有机物分子中最多可形成4个碳碳单键 | |
| D. | 蛋白质的水解和油脂的皂化都是由高分子生成小分子的过程 |
11.化学在生活中有着广泛的应用,下列做法错误的是( )
| A. | 采取低碳、节俭的生活方式 | |
| B. | 工业生产中用NaOH溶液吸收氮的氧化物 | |
| C. | 用风能、太阳能代替部分火力发电 | |
| D. | 食品工业生产中选用SO2作为漂白剂 |
9.下列物质的水溶液因水解而呈酸性的是( )
| A. | CH3COOH | B. | Na2SO4 | C. | NH4Cl | D. | KNO3 |
